Данная статья является реферативным изложением основной работы. Полный текст научной работы, приложения, иллюстрации и иные дополнительные материалы доступны на сайте VII Международного конкурса научно-исследовательских и творческих работ учащихся «Старт в науке» по ссылке: https://school-science.ru/7/13/40861.
Лимонная кислота, уксус, нашатырный спирт, известь, аскорбиновая кислота, щавелевая кислота – вещества, часто встречающиеся в быту. Среди кислот и щелочей много опасных, агрессивных веществ, способных вызвать тяжелые химические ожоги. Многие растворы кислот и щелочей бесцветны, не имеют запаха, их нельзя пробовать на вкус. Как же различить эти вещества? Из источников информации я узнал: чтобы различить кислоты и основания используют индикаторы.
Индикаторы – это органические и неорганические вещества, изменяющие свою окраску в зависимости от реакции среды. Название «индикаторы» происходит от латинского слова indicator, что означает «указатель».
Также я узнал, что индикаторы бывают синтетического и природного происхождения. Сегодня используются и технические средства для определения кислотности среды.
Я заинтересовался: «А какие растения могут использоваться для получения индикаторов? Можно ли приготовить растворы растительных индикаторов самостоятельно? Пригодны ли самодельные индикаторы для использования при проведении экспериментов?». Захотелось сравнить свойства самодельных и синтетических индикаторов, а также изучить среду некоторых веществ.
Цель работы: Исследование свойств синтетических индикаторов, применяемых в школьной лаборатории, и полученных из соков и отваров цветов, овощей, ягод, изучение характера среды с их помощью.
Гипотеза:
• растворы растительных индикаторов можно приготовить самостоятельно и применять в химической лаборатории и домашних условиях при необходимости определения среды раствора;
• свойства растворов индикаторов зависит от способа получения;
• растворы природных индикаторов помогут определить значение рН раствора с точностью универсального индикатора.
Для достижения поставленной цели необходимо решить следующие задачи:
• изучить литературные источники по теме;
• приготовить растворы индикаторов из природного сырья различными способами и исследовать влияние кислой и щелочной среды на их окраски;
• сравнить полученные данные со свойствами показателей кислотно-щелочной среды заводского универсального индикатора;
• провести исследование по определению среды растворов некоторых средств, применяемых в быту.
Объект исследования:
• растения, соки которых обладают свойствами индикаторов,
• синтетические индикаторы школьной лаборатории.
Предмет исследования: Кислотно-щелочные свойства отвара и сока цветов, ягод, овощей.
Задачи исследования:
• Эксперимент
• Наблюдение
• Сравнение
• Анализ полученных результатов и соотнесение его с гипотезой
1. Теоретическая часть
Прежде чем провести свои практические исследования, я должен был узнать, что представляют собой индикаторы, какие у них свойства. Поэтому я обратился к теоретическим источникам в этой области. Для этого я использовал ресурсы Интернета и книги.

1.1. Справка об основных индикаторах школьной лаборатории
Выделенные из растений пигменты – красящие вещества – были известны еще в Древнем Египте и Древнем Риме. Что же касается начала использования органических веществ в качестве индикаторов, то оно относится к XVII в. и связано с именем известного английского ученого – физика и химика – Роберта Бойля (1627–1691).
Лакмус
Еще в 1640 году ботаники описали гелиотроп – душистое растение с темно-лиловыми цветками, из которого было выделено красящее вещество. Этот краситель, наряду с соком фиалок, стал широко применяться химиками в качестве индикатора. Об этом можно прочитать в трудах Роберта Бойля. Однажды, изучая свойства соляной кислоты, закупленной в Германии у И.Глаубера, случайно пролил ее. Кислота попала на сине-фиолетовые лепестки фиалок. Спустя некоторое время лепестки стали ярко-красными. Это явление удивило Р.Бойля, и он тут же провел серию опытов с разными кислотами и цветами разных растений. Оказалось, что и васильки, и роза, и цветки некоторых других растений изменили свою окраску при действии кислот.

Вот что писал Р. Бойль о гелиотропе (Приложение рис. 1) – растении с душистыми темно-лиловыми цветами: «Плоды этого растения дают сок, который при нанесении на бумагу или материю имеют сначала свежий ярко-зеленый цвет, но неожиданно изменяет его на пурпурный. Если материал замочить в воде и отжать, вода окрашивается в винный цвет, такие виды красителя (их обычно называют «турнесоль») есть у аптекарей, в бакалейных лавках и в других местах, которые служат для окраски желе, или иных веществ, кто как хочет». [4, 11].
Роберт Бойль приготовил водный настой лакмусового лишайника для своих опытов. Склянка, в которой он хранил настой, понадобилась для соляной кислоты. Вылив настой, Бойль наполнил склянку кислотой и с удивлением обнаружил, что кислота покраснела. Заинтересовавшись этим, Бойль на пробу добавил несколько капель настоя лакмуса к водному раствору гидроксида натрия и обнаружил, что в щелочной среде лакмус синеет. Так был открыт первый индикатор для обнаружения кислот и оснований, названный по имени лишайника лакмусом.
Вначале с помощью лакмуса исследовали минеральные воды, а примерно с 1670 года его начали использовать в химических опытах. «Как только вношу незначительно малое количество кислоты, – писал в 1694 французский химик Пьер Поме о „турнесоле», – он становится красным, поэтому если кто хочет узнать, содержится ли в чем-нибудь кислота, его можно использовать». В 1704 немецкий ученый М.Валентин назвал эту краску лакмусом; это слово и осталось во всех европейских языках, кроме французского; по-французски лакмус – tournesol, что дословно означает «поворачивающийся за солнцем». Так же французы называют и подсолнечник; кстати, «гелиотроп» означает то же самое, только по-гречески.
По известным данным, для получения лакмуса растительное сырьё измельчают до порошкообразного состояния и в течение нескольких недель вымачивают в содово-аммиачном растворе (сода или поташ + NH4OH) при постоянном перемешивании. Раньше вместо раствора аммиака использовалась моча как источник ионов CO32– и NH4+. После отделения осадка полученный продукт высушивается и размалывается. В результате образуется порошок. Прессовка осадка с гипсом или мелом позволяет получить легко крошащиеся блоки готового сухого лакмуса [3].

Лакмус – красящее вещество, добываемое из некоторых видов лишайников (например, Roccella tinctoria). Состав лакмуса сложен и окончательно не установлен. Красящий компонент лакмуса – слабая кислота азолитмин, соли которой имеют синий цвет.
Лакмоид
Красящее вещество темно-фиолетового цвета (в чистом состоянии). Для приготовления его поступают следующим образом. Берут 100 частей резорцина, 5 ч. азотистокислого натрия NaNO2 и 5 ч. дистиллированной воды и постепенно нагревают в колбе на масляной бане до 1100. Он получается в виде блестящих красно-бурых зерен, легко превращаемых в порошок. Это и есть лакмоид. Он не растворим в бензоле и хлороформе; легко растворяется в метиловом, этиловом и амиловом спиртах, в ацетоне, уксусной кислоте в феноле; хуже в воде и эфире. Лакмоид напоминает лакмус, с кислотами он дает красное окрашивание, а со щелочами синее [13] (приложение 1, рис. 2–5).
Фенолфталеин
Фенолфталеин, который применяется в виде спиртового раствора, приобретает в щелочной среде малиновый цвет, а в нейтральной и кислой он бесцветен. (Приложение 1, рис 6–7).
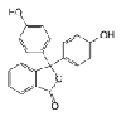
Фенолфталеин – трифенилметановый краситель, кислотно-основный индикатор, изменяющий окраску от бесцветной (при pH < 8,2) до красно-фиолетовой, «малиновой» (в щелочной); но в концентрированной щелочи – вновь бесцветен. В концентрированной серной кислоте образует розовый катион.
Вещество представляет собой бесцветные кристаллы, плохо растворимые в воде, но хорошо – в спирте и диэтиловом эфире.
Синтез фенолфталеина впервые осуществил в 1871 году немецкий химик Адольф фон Байер, будущий лауреат Нобелевской премии [15].
Метиловый оранжевый
Метиловый оранжевый, метилоранж, гелиантин – органический синтетический краситель группы азокрасителей. Применяют как кислотно-основной индикатор при титровании растворами сильных кислот, а также для определения водородного показателя (pH) среды. Переход окраски от красной к оранжево-жёлтой наблюдается в интервале значений pH 3,1—4,4. Метиловый оранжевый получают, диазотируя сульфаниловую кислоту, а затем сочетая полученное вещество с диметиланилином.

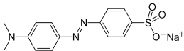
Что касается индикатора метилового оранжевого, он действительно оранжевый в нейтральной среде. В кислотах его окраска становится розово-малиновой, а в щелочах – желтой [12] (приложение 1, рис. 8–10).
Универсальный индикатор
В настоящее время химики часто пользуются индикаторной бумагой, пропитанной смесью разных индикаторов – универсальным индикатором. В азотной кислоте бумажка изменила свой цвет на тёмно-красный. Существуют другие кислоты, в которых бумажка меняет свой цвет на красный. Это серная кислота, соляная и др. Эти кислоты называются сильными кислотами. А такие кислоты, как уксусная, лимонная, винная и др., относящиеся, главным образом, к большому классу химических веществ – органических, называются слабыми. В таких кислотах бумажка приобретает розовый цвет.

Универсальная индикаторная бумага
Значит, с помощью индикаторной бумажки можно определить сильную и слабую кислоту, если они имеют раствор примерно одинаковой концентрации.
В растворе щёлочи бумажка меняет свой цвет на синий.
Универсальной индикаторной бумагой пользуются только для приближённого определения значений рН в широких пределах с точностью около одной единицы рН. (См. приложение рис 11–13).
1.2. Классификация индикаторов
Одни из самых распространенных – кислотно-основные индикаторы, изменяющие цвет в зависимости от кислотности раствора. Происходит это потому, что в кислой и щелочной среде молекулы индикаторов имеют разное строение. Примером может служить общеизвестный индикатор фенолфталеин. В кислой среде это соединение находится в виде недиссоциированных молекул и раствор бесцветен, а в щелочной среде – в виде ионов и раствор имеет малиновый цвет (приложение 1, табл. 1).
Помимо кислотно-основных применяют и другие типы индикаторов.
Окислительно-восстановительные индикаторы изменяют свой цвет в зависимости от того, что присутствует в растворе окислитель или восстановитель. Такими индикаторами служат вещества, которые сами подвергаются окислению или восстановлению, причем окисленная и восстановленная формы имеют разные окраски. Например, окисленная форма дифениламина имеет фиолетовую окраску, а восстановленная – бесцветную (приложение 1, табл. 2).
Широкое распространение получили комплексонометрические индикаторы – вещества, образующие с ионами металлов окрашенные комплексные соединения.
Некоторые вещества, адсорбируются на поверхности осадка, изменяя его окраску; такие индикаторы называются адсорбционными. Адсорбционные индикаторы – вещества, способные адсорбироваться на поверхности осадка и менять при этом окраску или интенсивность люминесценции. Эти индикаторы, как правило, обратимы и используются в осадительном титровании. В первую очередь осадком адсорбируются ионы, идентичные тем, которые входят в состав самого осадка, после чего адсорбируются индикаторы. Большая группа индикаторов – красители, адсорбирующиеся поверхностью осадка с образованием солей с ионами, содержащимися в осадке (приложение 1, табл. 3).
При определении среды мутных или окрашенных растворов, в которых практически невозможно заметить изменение окраски обычных кислотно-основных индикаторов, используют флуоресцентные индикаторы. Они светятся (флуоресцируют) разным цветом в зависимости от рН раствора. При этом важно, что свечение индикатора не зависит от прозрачности и собственной окраски раствора. При отсутствии фабричных химических индикаторов для определения среды растворов можно успешно применять самодельные индикаторы из природного сырья.
1.3. Растительные индикаторы
Растительные индикаторы содержат окрашенные вещества, способные менять свой цвет в ответ на то или иное воздействие. Называются эти окрашенные вещества пигментами. Их окраска определяется избирательным поглощением света в видимой части солнечного спектра. Меланин – пигмент, встречающийся кожуре красных сортов винограда, лепестках некоторых цветков. Пигмент является сильным антиоксидантом.
Фитохром – голубой растительный пигмент белкового строения, контролирует процессы цветения и прорастания семян. У одних растений ускоряя цветение, у других – задерживая. Известно, что строение пигмента меняется в зависимости от светлого и тёмного времени суток, сигнализируя об этом растению. Phyton – от греческого слова растение, сhrom – цвет, краска. Это вещество регулирует синтез белковых молекул (ДНК, РНК), образование хлорофилла, каратиноидов, антоцианов, органических фосфатов, витаминов. Фитохром связан с клеточными мембранами и встречается практически во всех органах растения.
Антоцианы – придают растениям окраску в диапазоне от розовой, красной, сиреневой, до синей и тёмно-фиолетовой. Антоцианы образуются в процессах гидролиза крахмала и по своему происхождению являются безазотистыми соединениями, близким к глюкозидам – соединениям сахара с неуглеводной частью. Антоцианы хорошо растворимы в воде и присутствуют в соке вакуолей. Диапазон цветов изменяется благодаря наличию в растении всего трёх моделей антоцианов, различных между собой числом гидроксильных групп. Вариации в пропорциях этих пигментов в растениях дают разную окраску лепестков. В зависимости от кислотности (рН) среды сока вакуолей, антоциан придаёт ту или иную окраску. В кислой среде он обычно имеет красные тона, например, у герани, гортензии, фиалок. В щелочной среде эти растения приобретают сине-голубые тона. Красная окраска – у маков, роз, герани, синяя – у васильков, голубая – у колокольчиков обусловлена наличием пигмента антоциана. Плоды винограда, слив, торна, краснокочанной капусты, свеклы окрашены антоцианом. Считается, что антоциан защищает растения от низких температур, от вредного воздействия солнечного цвета на цитоплазму.
Антоцианы сложные, неустойчивые соединения, в клетках растений обычно содержится несколько различных антоцианов, и проявление их связано с химическим составом почвы и возрастом растения. Поступая в организм человека с фруктами и овощами, антоцианы проявляют действие, схожее с витамином Р, они поддерживают нормальное состояние кровяного давления сосудов, предупреждая внутренние кровоизлияния [1,7].
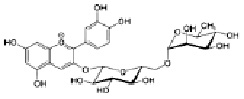
Антоциан костянок вишни
Антохлор – пигмент жёлтого цвета. Встречается в клетках кожицы лепестков первоцвета (баранчики, примула), льнянки, жёлтого мака, георгины, в плодах лимонов и других растениях. Антофеин – редко встречающийся пигмент тёмного цвета. Вызывает окраску пятен на крыльях венчика у русских бобов (Faba vulgaris). Каротиноиды – содержатся в растениях, устойчивых к пониженным температурам. Когда хлорофилл исчерпывается в холодное время года, листья приобретают заметную жёлтую или оранжевую окраску за счёт пролонгированного действия пигмента каротиноида. Каротиноиды защищают растения от пагубного действия солнечного света. Оранжево-красный цвет растениям даёт пигмент каротин, жёлтую – ксантофилл. Эти пигменты имеют белково-липоидную основу. Эти пигменты обнаружены в плодах помидоров, апельсинов, мандаринов, в корне моркови. Основная роль этих пигментов – придать растениям яркую привлекательную окраску, привлекая птиц и животных для разнесения семян. Цветы с оранжево-жёлтой окраской – лютик, настурция. [10]
1.4. Шкала рН и характер среды
Для определения характера среды используется рН-шкала. Термин рН образовался от датского слова potenz – степень и «Н» – символа водорода.
Численное значение водородного показателя (рН) в шкале от 0 до 14 характеризует концентрацию кислоты или щелочи в растворе. Значение 0 указывает на то, что раствор представляет собой сильную кислоту, среднее значение 7 соответствует нейтральному раствору, рН= 14 имеют сильные основания, или щелочи. В нейтральном растворе при 25°С рН = 7. В кислых растворах рН < 7, и тем меньше, чем кислее раствор; в щелочных растворах рН > 7, и тем больше, чем больше щёлочность раствора (приложение 1, табл. 4).
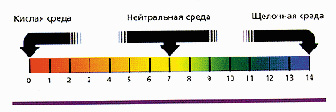
Индикаторы меняют свой цвет в зависимости от значения рН по-разному [3] (приложение 1 табл. 5).
1.5. Требования к индикаторам
Чтобы какое-либо вещество могло служить индикатором, оно должно удовлетворять следующим необходимым условиям:
должно быть слабой кислотой или слабым основанием;
его молекулы и ионы должны иметь разную окраску;
окраска их должна быть чрезвычайно интенсивной, чтобы быть заметной при добавке к испытуемому раствору малого количества индикатора.[8].
2. Практическая часть
2.1. Опыт № 1 «Получение растворов синтетических индикаторов и исследование их свойств»
Оборудование: химические стаканы, воронка, фильтровальная бумага, штативы, стеклянные палочки, колбы, капельницы.
Реактивы: лакмоид, фенолфталеин, метиловый оранжевый и индикаторные бумаги: универсальная и красная лакмусовая, этиловый спирт, дистиллированная вода.
Ход работы:
1. Приготовить раствор фенолфталеина в этиловом спирте, лакмоида и метилового оранжевого в воде.
2. Профильтровать и перелить готовые растворы в капельницы.
3. Исследовать свойства индикаторов в кислой и щелочной среде.
4. Наблюдения зафиксировать и сфотографировать полученные результаты.
Выводы по данному опыту:
1. Растворы синтетических индикаторов достаточно легко получить в школьной лаборатории при наличии твердых веществ.
2. Эти вещества меняют свой цвет в зависимости от среды раствора.
3. По изменившемуся цвету можно предсказать среду раствора и правила его использования.
4. Универсальная индикаторная бумага позволила определить значение рН испытуемых растворов (приложение 1, рис. 2–13).
2.2. Опыт №2 «Получение растительных индикаторов»
Сырье для получения растворов индикаторов:
1) лепестки цветов: розы, гвоздики
2) свежезамороженные ягоды: черника, смородина, малина, ежевика, клубника, вишня, облепиха, клюква;
3) овощи: краснокочанная капуста, столовая свекла, морковь, красный и желтый лук, чеснок;
4) листья петрушки и черной смородины.
Оборудование: ступка и пестик, химические стаканы, спиртовка, воронка, фильтровальная бумага, штативы, стеклянные палочки, колбы, водяная баня.
Ход работы:
1. Приготовим отвар: к 10 г. листкам цветов истертых в ступке добавим 50 г. воды и кипятим 1, 2 минуты. Полученный отвар отфильтровали, к полученному раствору добавили спирт (в отношении 2:1), чтобы лучше сохранить полученный раствор от закисания, образования плесени.
2. Аналогично образом приготовим отвар ягод, а отвар овощей варим 10 – 25 минуты на водяной бане.
3. Отварами полученных индикаторов пропитаем фильтровальную бумагу, высушим ее, поместив на стекло в темном месте. Через 2 дня индикаторная бумага готова к использованию [7, 8].
4. Из свежезамороженных фруктов и ягод, овощей выжали сок, для этого их натерли на терке или измельчили в ступке, после этого «отжали» через слой марли сок [9,10].
Выводы по результатам опыта
1. Растворы индикаторов, возможно, приготовить в домашних и лабораторных условиях;
2. Растворы получились ярко окрашенными.
3. Индикаторная бумага получилась качественной.(См. приложение 2, рис. 1– 13)
2.3. Опыт № 3 «Исследование окраски полученных растительных индикаторов в кислой и щелочной средах»
Оборудование; пробирки, стеклянные палочки, индикаторная бумага.
Реактивы: готовые растворы отваров растений, ягод и овощей, растворы кислоты и щелочи.
Ход работы:
1. Для проверки индикаторных свойств полученных растворов приготовили 100 г. 0,1% раствора HCI и 100 г. 0.1% раствора КOH. рН данных растворов определяли по изменению цвета универсального индикатора.
2. При добавлении нескольких капель полученных индикаторов в растворе HCI и КOH происходило изменение цвета индикаторов.
3. Результаты исследования занесены в дневник наблюдений (табл. 1).
4. Сделаны фотографии с результатами опыта.
Выводы по результатам опыта:
1. Природные индикаторы можно использовать для определения среды раствора
2. Большинство природных индикаторов в кислой среде изменяют свой цвет на красный или его оттенки, а в щелочной среде приобретают оттенки зеленого и желтого цветов.
3. Не все ягоды и растения можно использовать для получения кислотно-основных индикаторов
4. Лучшие индикаторы получились из растворов черники, вишни, свеклы, краснокочанной капусты, красного лука, ежевики, розы и гвоздик.
5. Лук желтый, чеснок, облепиха, листья черной смородины листья петрушки плохо подходят для получения природных индикаторов
6. Фотоотчет о результатах опыта в приложении 3 рис. 1– 17.
2.4. Опыт № 4 «Сравнение действия индикаторов, полученных из отвара и свежевыжатых соков свежих и замороженных ягод и овощей»
Оборудование: пробирки, стеклянные трубки.
Реактивы: свежевыжатые соки ягод и овощей, отвары ягод и овощей, раствор соляной кислоты, раствор гидроксида калия.
Ход работы: Для сравнения свойств индикаторов провели исследование растворов плодов и ягод, взятых в замороженном виде и свежих овощей.
1. Для исследования взяты замороженные ягоды смородины, черники, клубники, ежевики, вишни и клюквы. Из них готовили сок и отвар.
2. Заморозили свеклу и краснокочанную капусту в морозильной камере при температуре –15ºС.
3. Приготовили свежевыжатый сок свеклы, краснокочанной капусты, красного лука и отвары этих овощей.
4. Прикапывали одинаковое количество индикатора в пробирки с кислотой и щелочью
5. Сравнивали полученный результат и заносили его в дневник наблюдений (табл. 2).
Выводы по результатам опыта:
1. Свойства некоторых индикаторов зависят от способа хранения и вида ягод и плодов.
2. Более качественные изменения заметны при использовании выжатого сока ягод и плодов.
3. В щелочной среде происходит с течением времени изменение окраски индикаторов до желтого или коричневого цветов.
4. У соков изменение окраски в щелочной среде до коричневого оттенка происходит медленнее.
5. Для дальнейшего исследования гипотезы необходимо сверить результаты исследования летом, используя свежие ягоды.
6. Фотоотчет по результатам опыта – в приложении 4 рис. 1–8.
2.5. Опыт № 5 «Исследование изменения окраски индикаторов при разных значениях pH – среды в сравнении со свойствами универсального индикатора»
Оборудование: пробирки, стеклянные трубки, пластины для опытов с небольшим количеством веществ.

Реактивы: набор растворов, имеющих разные значения рН, растворы природных индикаторов.
Ход работы:
1. В ячейки пластины прокапаем по капле реагентов.
2. Добавим каплю индикатора.
3. Запишем полученные данные в дневник наблюдений (См. таблица 3).
4. Проанализируем данные.
Выводы по результатам опыта:
1. Полученные индикаторы растительного происхождения изменяют свой цвет в зависимости от значения рН, но интервал изменения цвета достаточно велик у многих природных индикаторов, в отличие от универсального индикатора.
2. Имея перед собой цветовую шкалу каждого индикатора можно определить при необходимости примерное значение рН исследуемого раствора.
3. При исследовании данных образцов индикаторов заметили особенное изменение цвета почти всех индикаторов в растворе, рН которого равно 4: все индикаторы приобретали необычайно пурпурную окраску.
2.6. Опыт № 6 «Обнаружение свойств растворов веществ, применяемых в быту с помощью кислотно-основных индикаторов»
Реактивы: Растительные индикаторы: черника, вишня, черная смородина, краснокочанная капуста, гвоздика и универсальная индикаторная бумага, вода.
Оборудование: химические стаканчики, стеклянные палочки, пробирки.
Ход работы: Каждое исследуемое чистящее и моющее средство растворим в воде и разделим на пять частей. В одну из них опустим универсальную индикаторную бумажку, во вторую каплю отвара черники, в третью-отвар вишни и т.д. В каждой из них индикаторы изменили окраску. Результаты записали в дневник наблюдений (табл. 4).
Выводы по результатам исследования:
1. Все индикаторы, самодельные и заводская универсальная бумага, показали во всех испытуемых средствах соответствующий характер среды.
2. Щелочную среду имеют Тайд , Sorti, Fairy, сода пищевая, нашатырный спирт.
3. Более щелочными оказались раствор нашатырного спирта и соды пищевой.
4. Из средств для мытья посуды более щелочной раствор у средства Sorti, по сравнению с Fairy (рН соды = рН Sorti), а на этикетке Фэйри и Sorti не указано негативное воздействие щелочной среды на кожу рук. Кожа рук имеет кислотную среду РН=5,5. При использовании моющих средств для посуды, имеющих щелочную среду нарушается нормальная кислотная среда кожи рук.
5. Для предохранения кожи рук от негативного воздействия моющего средства должны иметь значение, соответствующее значению pН эпидермиса. Значит, при применении моющих средств необходимо использовать резиновые перчатки.
Гель для душа и кондиционер для волос имеют слабокислотную среду, что соответствует гигиеническим требованиям к данным средствам.
6. Самые агрессивные по воздействию на кожу человека: Taйд (сильнощелочная среда) и Sanfor (сильнокислотная среда). Проверив индикатором стиральный порошок, можно определить изделия из каких тканей нужно стирать этим порошком, например, шелковые и шерстяные изделия не следует стирать в сильнощелочной среде.Taйд не имеет предупреждающей надписи, а производители Sonforа предупреждают о кислотах в составе продуктах и средствах безопасного использования.
Таким образом, используя индикаторы и природного происхождения и синтетические можно определить среду используемого средства или продукта питания, а значит чувствовать себя уверенней в мире окружающих нас веществ.
Заключение
Таким образом, в ходе исследования гипотеза полностью подтвердилась. Задачи исследования выполнены.
Проведя научно-исследовательскую работу, пришли к следующим выводам:
Растворы растительных индикаторов можно получить в домашних условиях и использовать в качестве кислотно-основных индикаторов для определения среды растворов.
Наиболее пригодны для получения индикаторов такие растения как свекла, красная роза, гвоздика, черная смородина, краснокочанная капуста, ежевика, черника, вишня. Свойства этих индикаторов сравнимы со свойствами универсальной индикаторной бумаги.
Индикаторы из растительного сырья лучше готовить в виде растворов соков. Можно использовать и замороженное сырье.
Используя индикаторы и природного происхождения и синтетические можно определить среду используемого средства или продукта питания, а значит чувствовать себя уверенней в мире окружающих нас веществ.
Полученные индикаторы можно использовать на уроках химии, на занятиях элективного курса, чтобы учащиеся имели представление о природных индикаторах и использовали их в своей жизни в будущем, так как синтетические индикаторы не всем доступны.
Работу с природными индикаторами можно продолжить, исследуя индикаторные свойства других растений.
Заметная разница в цветах некоторых соков замороженных и свежих ягод, требует дальнейшего изучения на примерах других ягод в летнее время года.
Библиографическая ссылка
Бородин И.И. ИССЛЕДОВАНИЕ СВОЙСТВ ИНДИКАТОРОВ ПРИРОДНОГО И СИНТЕТИЧЕСКОГО ПРОИСХОЖДЕНИЯ // Международный школьный научный вестник. 2019. № 4-2. ;URL: https://school-herald.ru/ru/article/view?id=1134 (дата обращения: 17.05.2026).
