1. Введение
Известно, что одним из продуктов реакции медного купороса и желтой кровяной соли является полупроницаемая мембрана ферроцианида меди (II), которая хорошо пропускает молекулы воды и не пропускает молекулы CuSO4. Такая избирательная проницаемость мембраны способствует протеканию процесса осмоса, характерного, в том числе и для жизнедеятельности растительной клетки [4, c.306]. А сам эксперимент, проведенный в XIX веке Морицем Траубе, продемонстрировал, что в неживой природе неорганических веществ можно найти такие химические соединения, которые при взаимодействии образуют совершенное подобие растительной клеточки, способной вбирать в себя одни вещества из окружающей среды и выделять другие. По теории Траубе, рост полученных им искусственных клеточек происходит вследствие внутреннего гидростатического давления (тургор), которое играет важную роль в жизни растений. Таким образом, клеточки Траубе принято считать моделям живой клетки [9].
Еще в 1750г. русский ученный М.В. Ломоносов получал с помощью желтой кровяной соли удивительные по окраске малорастворимые в воде соединения, которые иногда называют «ферроцианидными солями Ломоносова», или «ферроцианидные кустарники Ломоносова». Эти изумительные растения, похожие на нитевидные водоросли формируются благодаря образованию на поверхности кристалликов желтой кровяной соли полупроницаемой пленки [1, c.126-127].
Целью данной работы стало: получить искусственную полупроницаемую оболочку (пленка коллоида), формирующуюся на поверхности клеточки Траубе - модели живой клетки. Изучить сущность осмотических процессов и воздействие гипертонических, гипотонических и изотонических растворов на живые клетки.
Задачи исследования
- Изучить информацию по теме «Осмос, осмотическое давление»
- Познакомиться осмотической системой на основе растительной клетки.
- Исследовать роль Морица Траубе в изучении тугорного давления
- Узнать, что называется клеточка Траубе
- Провести эксперименты по получению клеточки Траубе двумя способами
- Ответить на вопрос: что произойдет с клетками крови, если их помесить в гипотонический или гипертонический раствор хлорида натрия?
2. Теоретическая часть
А) Понятие осмос
О?смос (от греч. ?σμος - толчок, давление) — процесс односторонней диффузии через полупроницаемую мембрану молекул растворителя в сторону большей концентрации растворённого вещества из объёма с меньшей концентрацией растворенного вещества. Впервые осмос наблюдал А. Нолле в 1748 году, однако исследование этого явления было начато спустя столетие [14, с.5].
Явление осмоса наблюдается при наличии двух систем с различной концентрацией веществ, где подвижность растворителя больше подвижности растворённых веществ. Важным частным случаем осмоса является осмос через полупроницаемую мембрану, когда они сообщаются с помощью полупроницаемой мембраны. В этом случае по законам термодинамики выравнивание концентраций происходит за счет вещества, для которого мембрана проницаема.
Полупроницаемыми называют мембраны, которые имеют достаточно высокую проницаемость не для всех, а лишь для некоторых веществ, в частности, для растворителя [13, с.228]. (Подвижность растворённых веществ в мембране относительно мала). Как правило, это связано с размерами и подвижностью молекул, например, молекула воды меньше большинства молекул растворённых веществ. Если такая мембрана разделяет раствор и чистый растворитель, то концентрация растворителя в растворе оказывается менее высокой, поскольку там часть его молекул замещена на молекулы растворённого вещества. Вследствие этого переходы частиц растворителя из отдела, содержащего чистый растворитель, в раствор, будут происходить чаще, чем в противоположном направлении. Соответственно, объём раствора будет увеличиваться (а концентрация вещества уменьшаться), тогда как объём чистого растворителя будет, соответственно, уменьшаться (рис.1).
При рассмотрении двух систем с различной концентрацией по сторонам полупроницаемой мембраны выравнивание концентраций в системе 1 и 2 возможно только за счет перемещения воды. В системе 1 концентрация воды выше, поэтому поток воды направлен от системы 1 к системе 2. По достижении равновесия реальный поток будет равен нулю [12, с.188]
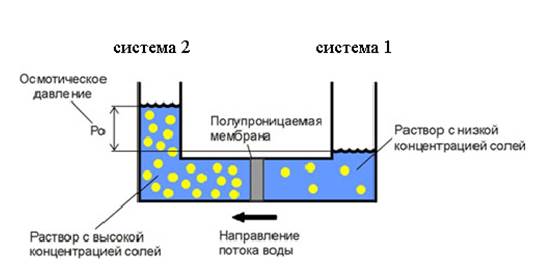
Рис. 1 Схема формирования осмотического давления
Осмос, направленный внутрь ограниченного объёма жидкости, называется эндосмосом, наружу - экзосмосом. Перенос растворителя через мембрану обусловлен осмотическим давлением. Это осмотическое давление возникает соответственно принципу Ле Шателье из-за того, что система пытается выровнять концентрацию раствора в обеих средах, разделённых мембраной, и описывается вторым законом термодинамики [16, c.190-194]. Оно равно избыточному внешнему давлению, которое следует приложить со стороны раствора, чтобы прекратить процесс, то есть создать условия осмотического равновесия. Превышение избыточного давления над осмотическим может привести к обращению осмоса - обратной диффузии растворителя.
В случаях, когда мембрана проницаема не только для растворителя, но и для некоторых растворённых веществ, перенос последних из раствора в растворитель позволяет осуществить диализ, применяемый как способ очистки полимеров и коллоидных систем от низкомолекулярных примесей, например электролитов [15, c.38-56].
Осмос играет важную роль во многих биологических процессах. Мембрана, окружающая нормальную клетку крови, проницаема лишь для молекул воды, кислорода, некоторых из растворённых в крови питательных веществ и продуктов клеточной жизнедеятельности; для больших белковых молекул, находящихся в растворённом состоянии внутри клетки, она непроницаема. Поэтому белки, столь важные для биологических процессов, остаются внутри клетки.
Осмос участвует в переносе питательных веществ в стволах высоких деревьев, где капиллярный перенос не способен выполнить эту функцию [3,с. 117].
Клетки растений используют осмос также для увеличения объёма вакуоли, чтобы она распирала стенки клетки (тургорное давление). Клетки растений делают это путём запасания сахарозы. Увеличивая или уменьшая концентрацию сахарозы в цитоплазме, клетки могут регулировать осмос [6, с.66]. За счёт этого повышается упругость растения в целом. С изменениями тургорного давления связаны многие движения растений (например, движения усов гороха и других лазающих растений).
Таким образом, осмос играет важную роль в жизни растительной клетки.
Б) Растительная клетка как осмотическая система
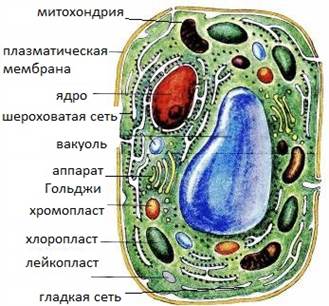
Рис.2 Растительная клетка
Растительную клетку можно рассматривать как осмотическую систему. Клеточная стенка обладает определенной эластичностью и может растягиваться. В вакуоли накапливаются растворимые в воде вещества (сахара, органические кислоты, соли), которые обладают осмотической активностью. Клеточный сок вакуоли является высококонцентрированным раствором. Тонопласт (от греч. tonos – натяжение, напряжение и plastos – оформленный, вылепленный) – мембрана, ограничивающая вакуоль растительной клетки [12, с.138].
Тонопласт и клеточная мембрана выполняют в данной системе функцию полупроницаемой мембраны, поскольку эти структуры избирательно проницаемы, и вода проходит через них значительно легче, чем вещества, растворенные в клеточном соке и цитоплазме [17, c.98].
Чтобы попасть в вакуоль, вода должна пройти через клеточную стенку, плазмалемму, цитоплазму и тонопласт. Клеточная стенка хорошо проницаема для воды [8, c.65]. Плазмалемма и тонопласт обладают избирательной проницаемостью, являются полупроницаемой мембраной, а вакуоль с клеточным соком – концентрированным раствором. Поэтому, если клетку поместить в воду, то вода по законам осмоса начнет поступать внутрь клетки.
Тургорное давление – внутреннее давление, которое развивается в растительной клетке, когда в неё в результате осмоса входит вода, и цитоплазма прижимается к клеточной стенке; это давление препятствует дальнейшему проникновению воды в клетку [6, с.66].
Эластическое растяжение ткани благодаря тургорному давлению ее клеток придает твердость неодревесневшим частям растений. Завядающие побеги становятся дряблыми, так как при потере воды тургорное давление падает. Тургорное давление противодействует притоку воды в клетку. Давление, с которым вода осмотически притекает в клетку, равно, таким образом, разности осмотического давления и тургорного давления.
В связи с этим, если клетка попадает в окружающую среду, где концентрация осмотически активных веществ (электролиты, неэлектролиты, белки) будет меньше по сравнению с концентрацией внутри клетки (или клетка помещена в воду), вода по законам осмоса должна поступать внутрь клетки.
Наблюдения за явлениями плазмолиза и тургора позволяют ученым изучать многие свойства клетки. Явление плазмолиза показывает, что клетка жива и протоплазма сохранила полупроницаемость. По скорости и форме плазмолиза можно судить о вязкости протоплазмы. Также явление плазмолиза позволяет определить величину осмотического давления (плазмолитический метод) [7, с. 135].
Осмотическое давление различно у разных жизненных форм. У древесных пород оно выше, чем у кустарников, а у кустарников выше, чем у травянистых растений. Разные экологические группы различаются по величине осмотического давления. Особенное значение имеет снабжение растений водой. У растений пустынь осмотическое давление больше, чем у степных растений. У степных — больше, чем у луговых. Еще меньше осмотическое давление у растений болотных и водных местообитаний. У светолюбивых растений осмотическое давление больше, чем у теневыносливых. Растение в определенной степени регулирует величину осмотического давления. Ферментативное превращение сложных нерастворимых веществ в растворимые (крахмала в сахара, белков в аминокислоты) приводит к возрастанию концентрации клеточного сока и повышению осмотического давления.
Однако, говоря о поступлении воды в клетку, надо учитывать, что наряду с осмотическим давлением в клетках существует давление набухания. Давление набухания связано со способностью гидрофильных коллоидов притягивать к себе молекулы воды. Сила, с которой коллоиды притягивают воду, и представляет собой давление набухания. Большое значение давление набухания имеет для молодых меристематических клеток, в которых отсутствуют вакуоли и которые заполнены коллоидным веществом [2, с.407].
В) Мориц Траубе, изучение тургорного давления

Мориц Траубе
(1826—1894)
Мориц Траубе (1826—1894) - немецкий химик-физиолог, брат профессора Людвига Траубе [5].
По окончании гимназии занимался в Берлине естественными науками и специально химией под руководством Е. Митчерлиха, Г. Розе и Раммельсбурга. Из Берлина Траубе перешел в Гиссен, где занимался в лаборатории Либиха. В 1846 г. Траубе. снова вернулся в Берлин, и через род получил степень доктора философии за химическую диссертацию "De nonnullis Chromii connubiis". Чтобы приобрести практические сведения. Траубе поступил на одну берлинскую красильню, но вскоре вернулся в Ратибор.
После смерти отца, он продолжал его дело (виноторговля) и досуги посвящал любимым занятиям теоретической химией. Его работы, сделанные в маленьком Ратиборе, вдали от общения с учеными, поразительны, отличаясь замечательной ясностью, логичностью мышления и новизной идей.
С 1851 по 1894 г. Траубе опубликованы 42 монографии, в которых он высказал совершенно новые взгляды на процессы брожения, нашедшие блестящее подтверждение в работах последних десятилетий. Процессы брожения вызываются, по мнению Траубе, не самими организмами брожения (дрожжами), но теми ферментами, которые эти организмы вырабатывают и выделяют в окружающую среду.
Громадное влияние на общую физиологию оказало открытие Траубе, касающееся образования растительных клеток. До того существовало представление, что в образовании, питании и росте клеток играют главную роль исключительно жизненные процессы.
Опыты Траубе показали, что можно найти такие неорганические химические соединения, которые при взаимодействии образуют совершенное подобие растительной клеточки, способной вбирать в себя одни вещества из окружающей среды и выделять другие. По теории Траубе, рост клеточек происходит вследствие внутреннего гидростатического давления (тургор).
Во внимание к трудам Траубе университет в Галле преподнес ему в день празднования своего 300-летнего юбилея в 1874 г., диплом на степень Dr. med. et chir. Не занимая никогда профессорского места, числясь корреспондентом Берлинской академии наук в течение всей своей жизни, Траубе не прерывал занятий наукой и умер среди начатых работ [5].
3. Практическая часть
А) Эксперимент с медным купоросом и желтой кровяной солью
Данный эксперимент имеет недостаток – в нём используются редкий, токсичный реактив – желтая кровяная соль [10, c.90]. Поэтому этот эксперимент ученики не смогут при желании повторить дома.
Используемые реактивы и оборудование:
- 5%-ный раствор медного купороса CuSO4;
- кристаллы желтой кровяной соли K?[Fe(CN)?];
- лимонная кислота HOOC-CH2-C(OH)COOH-CH2-COOH
- дистиллированная вода;
- химический стакан;
- пинцет
Ход работы:
В химическом стакане приготовим 5% раствор CuSO4. Для этого растворим при помешивании 15 г соли в 285 мл дистиллированной воды при комнатной температуре. Наблюдаем появление голубого мутного раствора CuSO4 в воде. Для подавления гидролиза сульфата меди по катиону в водном растворе, добавляем в стакан несколько крупинок лимонной кислоты. Наблюдаем, что раствор стал прозрачным. Это очень удобно для наблюдения процессов формирования клеточек Траубе.
После этого пинцетом поместим небольшой кристаллик желтой кровяной соли на дно стакана. Наблюдаем рост клеточки Траубе.


Рис.4. Рост клеток Траубе в растворе медного купороса.
Объяснение наблюдаемых процессов:
Рост искусственной клеточки Траубе основан на том, что подобно полупроницаемой мембране растительной клетки пленка ферроцианида меди (II) пропускает воду внутрь себя. Движущая сила - осмотическое давление, которое возникает из-за разности концентрации соли по сторонам мембраны.
2 CuSO4 + K4[Fe(CN)6] ®Cu2[Fe(CN)6] + 2 K2SO4
Концентрация желтой кровяной соли внутри клетки больше, чем концентрация сульфата меди снаружи. В результате вода проникает в клетку, тем самым увеличивая ее до тех пор, пока концентрации желтой кровяной соли и сульфата меди не уравняются. За счет давления мембрана из гексацианоферрата(II) меди постоянно разрывается. На месте разрыва опять взаимодействуют сульфат меди и желтая кровяная соль, и пленка образуется снова. Поэтому клеточка Траубе растет неравномерно.
Б) Эксперимент с хлоридом железа (III) и силикатным клеем
Данный эксперимент еще называется «Силикатный сад» и имеет преимущество перед предыдущим в плане большей доступности реактивов. Так силикатный клей можно приобрести в канцелярском магазине, а реактив FeCl3 в магазине для радиолюбителей (он используется при пайке радиодеталей). Поэтому этот эксперимент ученики смогут при желании повторить у себя дома неограниченное количество раз, наблюдая, как на скорость и размер «водорослей» влияет разная концентрация силикатного клея в воде и размеры кристаллов хлорида железа (III).
Реактивы и оборудование:
- силикатный клей;
- дистиллированная вода;
- хлорид железа (III)FeCl3;
- химический стакан
Ход работы:
Смешиваем силикатный клей и воду в соотношении 1:1. Насыпаем в полученный раствор немного соли FeCl3. Наблюдаем, как из кристалликов соли постепенно вырастают красивые «водоросли».


Рис.5. Рост клеток Траубе в силикатном растворе.
Объяснение наблюдаемых процессов:
Силикаты многих металлов плохо растворить в воде. Клей содержит относительно хорошо растворимые силикаты калия и натрия. В реакции обмена образуются силикаты железа, которые в водном растворе сразу же подвергаются гидролизу с образованием нерастворимого гидроксида железа (III)
2FeCl3 +3Na2SiO3 ® Fe2(SiO3)3 + 6NaCl
Fe2(SiO3)3 + 6H2O ® 2Fe(OH)3¯ + 3H2SiO3
Fe(OH)3¯ в виде пленки покрывает кристаллы соли FeCl3. Из кристалла опущенной соли вытягивается тоненькая полая трубочка, стенки которой состоят из образующегося осадка. Трубочка представляет собой полупроницаемую мембрану, внутри такой трубочки концентрация соли выше, чем снаружи. Наблюдается осмос - одностороннее перемещение вещества через полупроницаемую мембрану: вода устремляется внутрь оболочки. Какое-то время оболочка расширяется, но не выдерживает натиска и разрушается. В итоге соль FeCl3 снова контактирует с раствором силикатов, образуя новую пленку Fe(OH)3¯ . Благодаря этому «водоросль» растет.
4.Заключение
Клеточная мембрана живой клетки обладает свойством полупроницаемости. Это явление демонстрируется в опыте с искусственной клеткой Траубе.
В данной работе двумя независимыми способами была получена искусственная полупроницаемая оболочка (пленка коллоида), формирующаяся на поверхности клеточки Траубе - модели живой клетки.
Изучена сущность осмотических процессов и проведены эксперименты по воздействию гипертонических, гипотонических и изотонических растворов на живые клетки с применением модельной клеточки Траубе.
Сделано заключение о том, что получение клеточки Траубе с применением силикатного водного раствора и хлорида железа (III) более доступно и безопасно для школьников, чем способ с использованием медного купороса и желтой кровяной соли при проведении подобного эксперимента в домашних условиях.
Библиографическая ссылка
Ефимов В.М. ИЗУЧЕНИЕ ТУРГОРНОГО ДАВЛЕНИЯ В ЖИВОЙ КЛЕТКЕ С ИСПОЛЬЗОВАНИЕМ МОДЕЛИ - КЛЕТОЧКИ ТРАУБЕ // Международный школьный научный вестник. 2020. № 1. ;URL: https://school-herald.ru/ru/article/view?id=1273 (дата обращения: 15.03.2026).
