Изучение физико-химических процессов, реализующихся при фазообразовании и термических превращениях мелкодисперсных систем (МДС) с размером кристаллов от нескольких единиц до сотен нанометров является одной из актуальных проблем современной химии. Научный и практический интерес к таким системам обусловлен тем, что они по сравнению с аналогичными крупнокристаллическими объектами обладают специфическими, а порою и уникальными свойствами [4, 5, 7, 9, 11, 19-21]: магнитными; электрическими; повышенной реакционной способностью; пониженной температурой плавления и полиморфных превращений и др. Теоретические и экспериментальные исследования МДС свидетельствуют, что размер частиц определяет, наряду с другими термодинамическими параметрами, состояние мелкодисперсной системы.
Типичными представителями МДС являются оксидные соединения металлов с постоянной и переменной степенью окисления. Благодаря уникальным свойствам, они имеют широкое применение в промышленности, информационных технологиях, биотехнологиях и медицине. Особый интерес вызывают композиционные наноматериалы, обладающие новыми свойствами, которых нет ни у одного из компонентов в отдельности. Разработка таких материалов с новыми или улучшенными свойствами является актуальной задачей вследствие широкого развития промышленности и технологий.
Методы синтеза оксидных МДС многочисленны [22]. Особенностью оксидных соединений металлов является их малая растворимость [17], поэтому при их синтезе используют, как правило, методы кристаллизации из растворов с участием химических реакций, например, щелочной или термический гидролиз водных растворов солей металлов [6]. Для получения оксидных соединений металлов с переменной степенью окисления, наряду с гидролитическими, широко используется метод, основанный на окислении растворов солей или суспензий гидроксидов этих металлов [3].
Известно, что в гидротермальных условиях, то есть в замкнутом объёме, растворимость оксидных МДС возрастает, а это может оказывать инициирующее влияние на процессы фазо- и кристаллообразования труднорастворимых соединений. Однако, данный вопрос недостаточно полно освещен в литературе, что стимулировало проведение систематических исследований в этом направлении [19].
Объектом исследования: работы является композиционные материалы.
Предмет исследования: синтез композиционных материалов путем осаждения гидратированных оксидов (оксигидроксидов) Al(III) и Fe(II).
Цель и задачи исследований. Синтезировать и исследовать физико-химические свойства композиционных материалов в виде порошков на основе оксидов алюминия (III) и железа (II), полученных с использованием гидротермального метода.
Для достижения намеченной цели были поставлены следующие задачи:
1. Получение композиционного материала на основе оксидов (оксигидроксидов) алюминия (III) и железа (II) гидротермальным методом.
2. Изучить фазовый состав формирующихся продуктов;
3. Изучить влияние воды, оказываемое на структуру композиционных материалов при гидротермальной обработке в автоклаве.
4. Исследовать полученные композиционные материалы состава (α-Al2O3 и α-Fe2O3) на дифрактометре (ДРОН-3М), а также на сканирующем электронном микроскопе JEOL.
Методы и приемы:
1. Изучение литературного материала, обобщение, систематизация.
2. Аналитические методы (титрование, отстаивание, фильтрация).
3. Рентгенофазовый анализ (РФА).
4. Сканирующая электронная микроскопия (СЭМ).
Глава I. Литературный обзор
1.1. Структуры гидратированных соединений алюминия
Гидроксид алюминия γ – модификации (γ-Al(OH)3), встречающийся под названиями гидраргиллит или гиббсит, входит в состав природных бокситов, являющихся исходным сырьем в производстве алюминия [10, 13, 14].
Структура гидраргиллита построена из алюмогидроксильных слоев, гидроксильные группы которых образуют искаженную плотную упаковку (рис. 1.). Каждый ион алюминия внутри слоя окружен шестью ОН- группами, образующими искаженный октаэдр. Октаэдры сочленены между собой общими ребрами, образуя гексагональную сетку. Алюмогидроксильные слои связаны между собой водородными связями [13, 14].
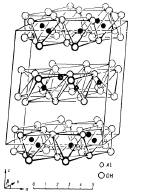
Рис. 1. Модель структуры гидраргиллита.
Оксигидроксид алюминия α – модификации (α – AlOOH), известен как минерал под названием диаспор. Название произошло от греческого слова «диаспора» – расстояние, вследствие распада минерала на мелкие куски при нагревании.
Диаспор кристаллизуется в рамках орторомбической сингонии и имеет структуру изоморфную минералу гетиту α-FeOOH (рис. 2.). Кристаллическая структура характеризуется плотной гексагональной упаковкой ионов O2-, причем ионы Al3+ размещаются в октаэдрических пустотах, т.е. между шестью ионами кислорода. Каждый ион кислорода связан с тремя ионами алюминия. Ионы Н+ располагаются между парами ионов кислорода, и в силу малости своих размеров не требуют большого пространства в кристаллической структуре. Таким образом, структура диаспора состоит из ионов алюминия и кислорода в соотношении 1:2 [10].
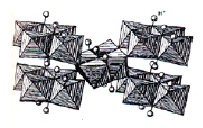
Рис. 2. Структура α – AlOOH (диаспор).
Непосредственный переход при термообработке диаспора в стабильную α- модификацию оксида алюминия (корунд) объясняется легкостью геометрического перехода структурных элементов диаспора в элементы структуры α – формы. Поэтому для перехода от структуры диаспора к структуре корунда необходимы минимальные геометрические преобразования октаэдров, не требующие диффузии катионов [13, 14].
Оксигидроксид алюминия γ- модификации (γ – AlOOH), известный как минерал бемит, можно получить осаждением аммиаком из водных растворов хлорида алюминия, либо прокалкой гидраргиллита в интервале 150 – 200°С, в результате которой образуется смесь бемита с рентгеноаморфной фазой переменного состава [12, 13, 14].
Бемит кристаллизуется в рамках орторомбической сингонии и имеет структуру изоморфную минералу лепидокрокиту или γ – FeOOH (рис. 3.).
Структура γ – модификации оксида алюминия относится к шпинели дефектного типа, и она существует благодаря наличию в ней стабилизирующей воды. С удалением воды при нагреве до 900-1000°С происходит переход в более высокотемпературную метастабильную θ – форму (моноклинный θ-Al2О3), и последующий переход в стабильную модификацию α-Al2О3 протекает довольно медленно (1100-1200°С) [13, 14].
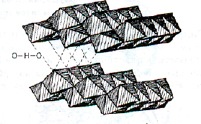
Рис. 3. Структура γ – AlOOH (бемит)
Корунд (α-Al2O3) изоморфен минералу гематит (α-Fe2O3) и кристаллизуется в рамках гексагональной сингонии (рис. 4.). В структуре корунда атомы кислорода, из-за высокой электроотрицательности, оттягивают электроны атомов алюминия из зоны проводимости на связь, стабилизируя тем самым устойчивые конфигурации sp2 и sp3. Ионы алюминия находятся в октаэдрическом окружении анионов кислорода [19]. Анионы кислорода в структуре корунда образуют гексагональную плотноупакованную решетку, в которой ионы алюминия занимают 2/3 октаэдрических пустот.
а) 
б) 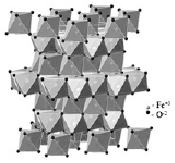
Рис. 4. Кристаллическая структура корунда (а) и гематита (б)
Оксиды алюминия и железа, а также их гидратированные формы, представляют собой большой класс неорганических соединений, хорошо распространенных в природе и используемых в различных приложениях.
1.2. Аппаратура для гидротермального синтеза
В методах гидротермального синтеза используются автоклавы – это кристаллизационные сосуды высокого давления. Автоклавы выдерживают высокие температуры и давления, в течение длительного периода времени. Стандартный автоклав представляет собой толстостенный, стальной сосуд со специальным герметически закрывающимся затвором.
Наиболее распространенной является модификация гидротермального метода, называемая методом перекристаллизации в условиях положительного температурного градиента. На дне автоклава, нагреваемого снизу и охлаждаемого сверху, размещается растворяемое вещество – шихта. В автоклаве создается разность температур (нижняя зона более горячая), чему способствует диафрагма – перегородка с отверстиями, разделяющая верхнюю и нижнюю зоны. Раствор циркулирует между гранулами шихты, насыщаясь веществом выращиваемого кристалла. Одновременно происходит нагревание гидротермального раствора. Горячий (и потому – более легкий) раствор поступает в верхнюю часть автоклава, где остывает.
Растворимость кристаллизуемого вещества с понижением температуры снижается, избыток растворенного вещества отлагается на затравки. Холодный высокоплотный обедненный раствор опускается в нижнюю часть автоклава и цикл повторяется. Процесс ведется до полного переноса вещества шихты на затравки. В результате этих процессов и растет кристалл. Выращиваемые монокристаллы обычно имеют высокое качество и характерную кристаллографическую огранку, так как растут в условиях более или менее близких к равновесным. Этот метод является основным для синтеза кварца, так могут быть выращены изумруд, корунд, малахит и другие минералы [12]. Для цилиндрических затворов в верхней части автоклава высверливается «гнездо» в виде цилиндра диаметром несколько больше, чем диаметр внутренней полости автоклава.
Поверхность «гнезда» тщательно шлифуется. Внешний диаметр медной прокладки «кольца» и стального кольца должен соответствовать диаметру «гнезда». Первоначальное уплотнение в цилиндрическом затворе создается за счет раздавливания натяжной гайкой медного кольца. В дальнейшем по мере роста внутреннего давления обтюратор двигается вверх и сдавливает медное кольцо. Такие затворы получили широкое распространение в гидротермальных реакторах вследствие их надежности и возможности длительной эксплуатации. Для предотвращения слипания нажимной гайки с корпусом реактора автоклава под действием высокой температуры и давления, перед опытом резьбу смазывали маслянистой графитовой суспензией (рис 5.).
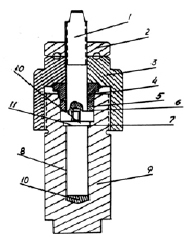
Рис. 5. Автоклав со сменной футеровкой:
1 – обтюратор,
2 – гайка нажимная,
3 – упорная гайка,
4,5 – упорные кольца,
6 – прокладка (медь),
7 – пробка,
8 – вкладыш,
9 – корпус,
10 – подставка,
11 – крышка вкладыша.
1.3. Применение оксидных соединений алюминия
Из гидроксида алюминия можно получить практически все соли алюминия. Так, например, безводный хлорид алюминия используется в химической практике в качестве катализатора при переработке нефти [22].
Кроме того, гидроксид алюминия является прекурсором при синтезе мелкодисперсного α-Al2O3, микропорошок на основе корунда или микрокорунда). Микрокорунд, обладая высокой твердостью уступающей только алмазу, является перспективным абразивным материалом. Абразивные микропорошки на основе корунда широко используются в шлифовально-полировальном инструменте, шлифовальной шкурке, полировальных пастах, а также в виде свободных абразивных зерен, для обработки изделий из металла, стекла, пластмассы, природного и искусственного камня [10].
Оксидные соединения алюминия широко применяются для синтеза керамических материалов. Алюмооксидная керамика обладает рядом ценных качеств – малой плотностью (в 3-6 раз меньше чугуна, молибдена или вольфрама), малым коэффициентом термического расширения, низкой теплопроводностью (~ в 3 раза ниже, чем у металла), высокой твердостью, тугоплавкостью, коррозионной устойчивостью. Специальная керамика сохраняет высокую механическую прочность до 1400°С. Эти свойства конструкционной керамики создали широкие возможности ее использования в самых различных областях техники.
В последнее время интенсивно развивается такое направление, как получение изделий на основе наноразмерного порошка оксида алюминия с поверхностями и режущими кромками невосприимчивыми к химически агрессивным средам [12]. Эти изделия позволяют заменить такие металлические элементы конструкций как: сменные насадки режущих поверхностей хирургического инструмента; ножницы для обрезки кевларовой защиты оптоволокон; щипцы, ножницы и лезвия для парикмахерской индустрии.
Глава II. Экспериментальная часть
2.1. Используемые материалы и оборудование
В работе были использованы следующие реактивы:
– октадекагидрат сульфата алюминия Al2(SO4)3 • 18H2O марки «ч.д.а», ГОСТ 3758-75
– гептагидрат сульфата железа (II) FeSO4 • 7H2O марки «ч.д.а.», ГОСТ 4148-78
– гидроксид натрия NaOH марки «ч.д.а», ГОСТ 4328-77
– дистиллированная вода ГОСТ 6709-72.
Все образцы взвешивались на аналитических весах «Mettler Toledo» AB204-S. Контроль рН проводился на универсальном pH-метр «Иономер «Эксперт-001», откалиброванном по двум буферным растворам. Все измерения рН растворов проводили при температуре 25±0,5°С. Буферные растворы готовили из фиксаналов: калий тетраоксалат (рН=1,68 при 25°С), тетраборат натрия (рН=9,18 при 25°С). В качестве измерителя использовался комбинированный электрод марки ЭСЛ-63-07, электрода сравнения – насыщенный хлорсеребряный.
Рентгенофазовый анализ проводили на дифрактометре ДРОН-3М фильтрованное СuКα – излучение, с автоматической записью кривых распределения интенсивности и скоростью съемки 1°/мин и 2°/мин (г. Челябинск, ЧелГУ). Идентификацию пиков на дифрактограммах и расчет параметров элементарной ячейки проводили с помощью программного комплекса PDWin 4.0, а также с помощью кристаллографической и кристаллохимической базы данных для минералов и их структурных аналогов WWW-МИНКРИСТ.
Состав образцов определяли на сканирующем электронном микроскопе высокого разрешения JEOL-7100F (длина волны 0,025 A, г. Челябинск, ЮУРГУ).
2.2. Соосаждение гидратированных оксидов Al(III) и Fe(II)
Соосаждение гидратированных оксидов Al(III) и Fe(II) осуществлялся при значении pH 7,02. В плоскодонную колбу объемом 250 мл насыпали 12,385 г сульфата алюминия и растворяли в 125 мл воды. Во вторую колбу объемом 50 мл взвешивали и насыпали 0,351 г сульфата железа и растворяли в 5 мл воды. Полученные растворы сливали друг с другом и осаждали соответствующим количеством раствора гидроксида натрия. Перемешивание производили в химическом стакане на магнитной мешалке. Полученные образцы промывали дистиллированной водой на воронке Бюхнера и сушили на воздухе в течение суток.
Затем, навески полученных соосаждением образцов по 1 г помещали в стальные капсулы (автоклавы). В-первый автоклав вносился исходный образец без добавления дистиллированной воды, а во-вторую добавляли 1 мл дистиллированной воды. Автоклавы с образцами помещали в предварительно нагретую муфельную печь. Температуру контролировали термодатом подключенным к муфельной печи. Температура термообработки составляла 450 С, точность ее поддержания составляла ± 2 С. Время термообработки составила – 4 ч. При выполнении работы использовали методы рентгенографии и сканирующей электронной микроскопии.
Глава III. Результаты и их обсуждения
3.1. Рентгенофазовый и электронный анализ полученных образцов
Рентгенографическая съемка образцов была произведена на приборе ДРОН-3М фильтрованное СuКα – излучение, с автоматической записью кривых распределения интенсивности. По данным рентгенографии полученный образец системы СОГ был рентгеноаморфным.
На рентгенограмме образца после гидротермальной обработки аморфного гидроксида без добавления воды, не наблюдалось дифракционных максимумов (рис. 6.).
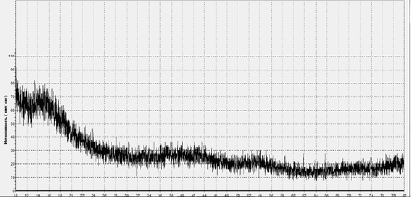
Рис. 6. Образец, аморфного гидроксида алюминия после гидротермальной обработки полученный при значении pH=7.02 без добавления воды.
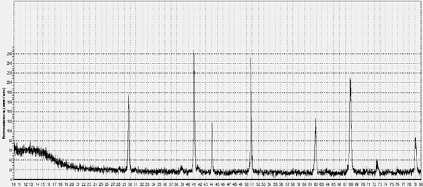
Рис. 7. Образец шпинели после гидротермальной обработки полученный при значении pH=7.02 с добавлением 1 мл дистиллированной воды
На рентгенограмме образца после гидротермальной обработки с добавлением 1 мл дистиллированной воды наблюдается совокупность дифракционных максимумов, принадлежащих к фазе оксида алюминия α – модификации, т.е. α – Al2О3, известную в литературе как корунд. Причем, на рентгенограмме присутствовали следы дополнительных рефлексов, которые можно отнести к фазе оксида железа (III) a- модификации (гематит) (рис. 7.).
Все полученные образцы, включая исходные, были сняты на сканирующем электронном микроскопе высокого разрешения JEOL-7100F в лаборатории «нанотехнологий» ЮУРГУ (рис. 8, 9, 10).
На электронных микрофотографиях (рис. 8, 9) исходного образца не наблюдается четко выраженной структуры.

Рис. 8. Микрофотография образца системы СОГ полученного при значении pH=7,02 при увеличении х2000

Рис. 9. Микрофотография образца шпинели после гидротермальной обработки без добавления воды, полученный при значении pH=7,02 при увеличении х500.

Рис. 10. Микрофотография образца шпинели после гидротермальной обработки с добавлением 1 мл воды, полученный при значении pH=7,02 при увеличении х10000.
На электронной микрофотографии (рис. 10.) полученного образца корунда, наблюдаются пластинчатые кристаллы однородного контраста, обладающие гексагональной огранкой со средним размером ~ 1 мкм в поперечнике и толщиной 150-200 нм.
Можно предположить, что образующиеся вначале кристаллики α – Fe2О3 выступают в качестве зародышей для термодинамически более устойчивой фазы α – Al2О3, что и приводит, в конечном счете, к формированию микрокристаллического монодисперсного корунда.
Выводы
Таким образом, при соосаждении растворов солей Al(III) и Fe(II) способствует формированию монодисперсного микрокорунда с гексагональной огранкой в гидротермальных условиях. Известно, что гематит изоструктурен с корундом, поэтому образующиеся сначала кристаллики α-Fe2О3 выступают в качестве зародышей для термодинамически более устойчивой фазы α-Al2О3, что и приводит, в конечном счете, к формированию микрокристаллического монодисперсного корунда без образования твердого раствора.
В результате термической обработки в автоклаве при 450°С воздушно-сухих соосажденных гидратированных оксидов Al(III) и Fe(II) без добавления дистиллированной воды наблюдается формирование слабокристаллической, практически аморфной фазы.
Показано инициирующее влияние воды, дополнительно вводимой в реакционную зону, на процесс кристаллообразования микрокорунда, в то время как соединения железа способствуют формированию пластинчатой формы кристаллов.
Библиографическая ссылка
Пасечник Д.Д., Клинчина Д.В. ПОЛУЧЕНИЕ И ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА МАТЕРИАЛОВ НА ОСНОВЕ НАНОДИСПЕРСНЫХ ОКСИДОВ АЛЮМИНИЯ (III) И ЖЕЛЕЗА (II) // Международный школьный научный вестник. 2018. № 5-2. ;URL: https://school-herald.ru/ru/article/view?id=669 (дата обращения: 26.01.2026).
