Лекарственный препарат Прегабалин (торговые названия: «Лирика®», «Прегабалин», «Альгерика», «Реплика») нашел широкое применение в медицине как противосудорожное и анальгезирующее средство. Лекарственная форма прегабалина – капсулы, в аптечных организациях стоит на предметно-количественном учете, отпускается из аптек по рецепту врача.
При применении прегабалина в терапевтических дозах отмечена хорошая переносимость препарата. Однако уже на стадии исследования зависимости было отмечено эйфоризирующее действие у больных, злоупотребляющих седативными средствами и алкоголем.
Начиная с 2008 г. регистрируются случаи немедицинского применения препарата, чаще наркозависимыми лицами, в завышенных дозировках для получения схожего с наркотическим действия, для «усиления» эффекта наркотических и других психоактивных средств, а также с целью купирования абстинентного синдрома после прекращения приема наркотиков. Результатом данного применения может быть острое или смертельное отравление.
Вследствие данных процессов существует потребность в разработке методик определения прегабалина высокочувствительными и специфичными методами.
Цель нашего исследования – разработка методики определения прегабалина методом обращено-фазовой высокоэффективной жидкостной хроматографии (ОФ ВЭЖХ).
Для достижения поставленной цели необходимо решить следующие задачи:
1. Изучить данные литературы о лекарственном препарате прегабалин, его медицинском и немедицинском применении, методах его анализа
2. Выбрать оптимальные условия определения прегабалина методом ОФ ВЭЖХ (подобрать состав хроматографической системы, режим хроматографирования, скорость потока элюент, аналитическую длину волны), установить основные хроматографические параметры прегабалина (время удерживания)
3. Оценить линейную зависимость аналитического сигнала от концентрации определяемого вещества в анализируемой пробе
Научная новизна – предложена методика определения прегабалина методом ОФ ВЭЖХ после переведения его в соединение, обладающее большим светопоглощением (реакция с дансилхлоридом) с применением отечественного жидкостного микроколоночного хроматографа «Милихром А-02».
Практическая значимость исследования заключается в том, что разработанная методика определения прегабалина может быть использована для фармацевтического анализа (определение прегабалина в лекарственных формах), а также в химико-токсикологическом анализе с целью его идентификации в образцах (биологические жидкости – моча, кровь, ткани внутренних органов) и вещественных доказательствах.
Степень изученности темы. В литературе имеются разрозненные данные о методах и методиках анализа прегабалина. Автором предложена ВЭЖХ-методика обнаружения прегабалина, пригодная для его идентификации и количественного определения в различных объектах.
Личный вклад автора. Автор самостоятельно осуществляла все этапы экспериментальной работы, включая приготовление реагентов, подвижной фазы, анализируемых растворов, подготовку и работу на аналитическом оборудовании, осуществляла сбор и обработку полученной информации, а также ее интерпретацию. Осуществила поиск и анализирование периодической и научной литературы по изучаемой тематике. Грамотно, научным языком оформила текст научной работы.
Глава 1. Обзор литературы
1.1. Применение прегабалина
в медицине, показания
и противопоказания
Прегабалин широко применяется в медицинской практике, является производным гамма-аминомасляной кислоты ((S)-3-(аминометил)-5-метилгексановая кислота). Основное действие связано с проявлением анальгезирующего, противосудорожного, анксиолитического эффектов.
Применение прегабалина показано при лечении нейропатической боли, фибромиалгии и генерализованного тревожного расстройства, в качестве дополнительной терапии эпилепсии с парциальными судорожными припадками. Препарат применяют внутрь, независимо от приёма пищи, в дозе от 150 до 600 мг/сут в 2 или 3 приема [5, 7, 9, 10, 12, 18, 22, 24, 28, 33, 34, 36].
Прегабалин быстро всасывается после приёма внутрь. Биодоступность прегабалина при приёме внутрь составляет более 90%. Соединение не связывается с белками плазмы крови, практически не подвергается метаболизму, выводится в основном почками в неизмененном виде.
Прегабалин противопоказан пациентам с непереносимость галактозы, лактазной недостаточность, в детском и подростковом возрасте до 17 лет [7].
Из нежелательных побочных эффектов отмечаются: головокружение, сонливость, нарушение внимания, ухудшение памяти, тремор, судороги; со стороны психики – эйфория, снижение либидо, бессонница, раздражительность. Пациенты с лекарственной зависимостью в анамнезе нуждаются в тщательном медицинском наблюдении на предмет симптомов зависимости от прегабалина.
1.2. Применение прегабалина в немедицинских целях
Несмотря на широкое применение в медицине и положительные эффекты при лечении заболеваний, регистрируются случаи использования прегабалина в немедицинских целях, а именно: купирование абстинентного синдрома, сочетание с наркотиками, психоактивными веществами для усиления наркотического эффекта, сочетание с алкоголем для усиления его эффекта.
При злоупотреблениях дозировки препарата составляли в среднем 1 г прегабалина в сутки (5-10 капсул на прием), обычно препарат принимали перорально, также встречались случаи внутривенного введения содержимого капсул после растворения или вдыхания через нос.
Прегабалин появился на фармацевтическом рынке в 2006 г. Первый случай злоупотребления препаратом зафиксирован в Швеции в 2008 г. В последующие годы был отмечен рост применения прегабалина с немедицинскими целями. В 2010-2012 гг случаи описаны также в США, Франции, Германии и Турции. С 2012 г такие факты стали регистрироваться на территории России.
Исходя из клинического опыта, врачи отмечают возможность формирования зависимости от прегабалина, вначале психической, а затем и физической зависимости. Нередко это пациенты с химической зависимостью и депрессивным состоянием. В случае длительного употребления препарата в высоких дозах возникает стойкая и выраженная эйфория. И это обязательно приводит к желанию повторного приема прегабалина.
Зависимость от прегабалина не имеет особых диагностических признаков. Для состояния опьянения характерны, в том числе, спутанность сознания, растормаживание, приподнятое настроение. Все эти обстоятельства популяризируют его немедицинское применение среди населения, в связи с чем, проблема токсикологического анализа приобретает высокую социальную значимость [6, 8, 15, 16 ,17, 20, 25, 26, 27, 30, 32, 35].
В данный момент времени ужесточены правила отпуска производных γ-аминомасляной кислоты, в частности, прегабалина, данный препарат из аптечной организации отпускается только при предъявлении рецепта [21].
1.3. Методы определения аминокислот, их производных и прегабалина
В литературных источниках встречается информация о методах определения аминокислот, пептидов, а также прегабалина
Аминокислоты и их производные определяют методом ВЭЖХ, в качестве реагентов для получения дериватов используются: нингидрин, о-фталевый альдегид (возможны сочетания с этантиолом или 2-меркаптоэтанолом), фенилизотиоционат, 1-нафтилизоционат, 9-флоренил-метилхлороформиат, дабсилхлорид (4-диметил-аминоазобензол-4`- сульфонил хлорид). Разделение дериватизированных аминокислот осуществляют на обращенно-фазовых колонках, заполненных силикагелем с привитыми группами С8 или С18. В качестве подвижных фаз применяются смеси буферных растворов (фосфатные, цитратные, ацетатные – рН 4,5-7,2) с ацетонитрилом и (или) метанолом, реже – смеси буферных растворов с октансульфонатом натрия или тетрагидрофураном, раствор меди (ІІ) сульфата [23, 27].
Предложены варианты определения аминокислот без получения их дериватизированных производных. В этом случае детекция осуществляется в УФ-свете, рефрактометрическим или электрохимическим методом.
Для определения аминокислот используется химический метод с выполнением реакций: этерификации, конденсации с альдегидами и кетонами с образованием оснований Шиффа, ацилирования, диазотирования, с 1,2-нафтохиноном-4-сульфокислоты (реагентом Эрлиха-Гертера), окислительного дезаминирования, нингидриновая реакция.
Описаны методики спектрофотометрического определения прегабалина: взаимодействие прегабалина как первичного амина с аскорбиновой кислотой в присутствии диметилформамида, в результате получается окрашенный продукт (фиолетовый) с максимумом поглощения при 530 нм; взаимодействие прегабалина с салициловым альдегидом при pH 7,0 (продукт желтого цвета) с максимумом поглощения при 410 нм. Эти методы подходят для определения прегабалина в субстанции, в капсулах заводского производства.
Ещё один метод основан на конденсации прегабалина с 1,2-натрий нафтахинон-4-сульфокислоты в щелочной среде с получением продукта оранжевого цвета, и измерением оптической плотности при длине волны 353 нм. Этот метод был использован для оценки качества пяти препаратов прегабалина и в образцах человеческой мочи [29, 31].
Для пептидов и аминокислот в настоящее время активно применяется ОФ ВЭЖХ. Но, для того, чтобы уменьшить взаимодействие пептидов с остаточными силанольными группами, и одновременно улучшить взаимодействие с гидрофобной поверхностью неподвижной фазы в элюент добавляют сильные кислоты или соли. Для уменьшения полярности пептидов хроматографирование следует проводить при низких значениях рН (ниже 3).
В качестве растворителей для пептидов используют 0,1% растворы трифторуксусной и муравьиной кислот. Элюирование пептидов в ОФ ВЭЖХ, как правило, проводится в градиентном режиме с добавлением органического модификатора, чаще ацетонитрила [1, 2, 4, 19].
В работах Шуниной М.В. с соавт., Чернобровкина М.Г. с соавт. для определения аминокислот методом ОФ ВЭЖХ рекомендован их предварительный перевод в активные соединения с помощью органического реагента 5-диметиламинонафталин-1-сульфонилхлорид (дансилхлорид). Дансильные производные обладают высоким светопоглощением и флуоресценцией, поэтому для их определения пригодны спектрофотометрический или флуориметрический детектор. Оптимальное значение рН для прохождения реакции составляет 9,5-9,6 с использованием буферных растворов (боратный буфер с рН 9,6 и 9,0; литий-карбонатный буфер с рН 9,5; натрий гидрокарбонатный буфер с рН 9,5), при комнатной температуре в затемненном месте в течение 40-50 мин [3, 13].
1.4. Определение линейности методик
Под линейностью методики понимают наличие линейной зависимости аналитического сигнала от концентрации или количества определяемого вещества в анализируемой пробе в пределах аналитической области методики.
Для этого определяют рабочий диапазон концентраций образца, и проводят эксперименты по измерению аналитических сигналов для не менее чем 5 проб с различными концентрациями образца. В пределах указанного диапазона должна наблюдаться корреляция между аналитическим сигналом (площадь, высота, величина оптической плотности и др.) и концентрацией анализируемого соединения.
Чаще всего используется градуировочная модель – модель наименьших квадратов (метод линейной регрессии). Экспериментальные данные обрабатываются по данному методу с использованием линейной модели:
y = b × x + a, где x – количество/концентрация определяемого вещества; y – величина аналитического сигнала (отклика); b – угловой коэффициент; a – свободный член.
Должны быть рассчитаны и представлены величины b, a и коэффициент корреляции r. В большинстве случаев используют линейные зависимости, отвечающие условию |r | ≥ 0,99, и только при анализе следовых количеств допускается |r | ≥ 0,9 [11, 14].
Глава 2. Объект исследования, материалы и методы
2.1. Объект исследования
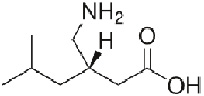
Прегабалин – (S)-3-(аминометил)-5-метилгексановая кислота, М.м.=59,23
Прегабалин – белое кристаллическое вещество, Тпл. 186 - 188 °С; легко растворим в воде, в растворах кислот и щелочей; лекарственная форма – капсулы 25, 50, 75, 100, 150, 200, 300 мг. Готовили рабочий раствор прегабалина с концентрацией 1,5 мг/мл (водный раствор).
2.2. Материалы, реактивы
1. Боратный буферный раствор рН 9,6: в мерную колбу на 200 мл отмеряли 50 мл раствора борной кислоты 0,2 моль/дм3 с калия хлоридом (1,237 г борной кислоты и 1,491 г калия хлорида растворяли в воде очищенной в мерной колбе на 100 мл) и 36,85 мл раствора натрия гидроксида 2 моль/дм3 (0,40 г натрия гидроксида растворяли в воде очищенной в мерной колбе на 50 мл), доводили водой очищенной до метки, перемешивали.
2. Дансилхлорид (5-диметиламино-
нафталин-1-сульфонилхлорид, М.м. = 269,75): порошок светло-коричневого света. Готовили раствор с концентрацией 0,75 мг/мл, растворитель ацетонитрил:вода (7:3), раствор использовали в день приготовления.
3. Подвижная фаза для ВЭЖХ (элюент): раствор трифторуксусной кислоты 0,1%: ацетонитрил.
Материалы: весы лабораторные общего назначения; пипетки, вместимостью 1, 2, 5, 10 мл; дозаторы автоматические 1-10 мкл, 25-100 мкл; колбы мерные, вместимостью 25, 50 мл (ГОСТ 1770); пробирки мерные, объемом 10, 25, и 50 мл; цилиндры мерные, вместимостью 25, 100 мл; стаканчики стеклянные, вместимостью 25, 50 мл; воронки; фильтры бумажные; стеклянные камеры для хроматографирования.
2.3. Характеристика аналитического оборудования
При проведении исследований методом высокоэффективной жидкостной хроматографии (ВЭЖХ) использовали жидкостный микроколоночный хроматограф «Милихром А-02» (г. Новосибирск, ЗАО Институт хроматографии «ЭКОНОВА»). Прибор представляет собой аналитический комплекс функционально объединённых устройств, обеспечивающий разделение жидких смесей веществ методом ВЭЖХ, детектирование, идентификацию и количественный анализ компонентов. Технические характеристики прибора:
Детектор – двухлучевой УФ-спектрофотометр (190-360 нм), одно- или многоволновая детекция, возможность снятия спектров поглощения.
Автоматический дозатор – дозируемый объём: 1…99 мкл.
Насос – шприцевой, сдвоенный, градиентный, программируемый линейно – кусочный градиент любой формы (до 20 участков).
Колонка – стальная колонка с обращенно-фазным сорбентом ProntoSIL С18, размер 2 х 75 мм, сорбент – 5 мкм, термостатирование колонки 35-90 °С.
Полное управление хроматографом от IBM PC под WINDOWS.
В работе применили хроматографические условия «База данных 2003». Методики формирования и использования программы «БД-2003» аттестованы Государственным комитетом РФ по стандартизации и метрологии в соответствии с требованиями ГОСТ Р 8.563-96 и ГОСТ Р ИСО 5725-2002. К настоящему времени в БД-2003 включены более 500 соединений.
Полученные хроматограммы обрабатывали с помощью программы обработки данных «АЛЬФАСПЕКТР» с вычислением для каждого вещества объема удерживания (VR, мкл), площади и высоты пика
Глава 3. Выбор условий определения прегабалина методом ВЭЖХ
Для разработки методики анализа изучаемого вещества методом ВЭЖХ необходимо было правильно выбрать состав подвижной фазы, рабочую длину волны детектирования, скорость потока элюента, температуру колонки.
3.1. Обоснование выбора сорбента
и подвижной фазы (элюента)
Применение сорбентов с модифицированной поверхностью по сравнению с разделениями на непривитом силикагеле позволяет быстро устанавливать равновесие сорбента с элюентом, что обеспечивает воспроизводимость результатов. При использовании полярных элюентов растворимость большинства соединений увеличивается.
Устройство жидкостного хроматографа «Милихром А-02» предусматривает термостатирование колонок. Температура в колонке должна быть оптимальна и постоянна от анализа к анализу для достижения максимально возможной воспроизводимости величин удерживания. По этим причинам эксперимент проводили при температуре 35-40 0С.
При выборе подвижной фазы нами учитывались физические и химические свойства её компонентов, которые оказывают влияние на константы равновесия и, соответственно, регулируют времена удерживания.
В качестве растворителей нами использованы базовые растворители, применяемые в обращенно-фазовой хроматографии: вода, буферные растворы, ацетонитрил.
3.2. Хроматографирование прегабалина в условиях «БД-2003»
Нами проведены исследования по определению прегабалина в условиях «БД-2003», где в качестве элюента используется смесь двух растворителей с заведомо более слабой – растворитель А (буферный раствор) и с заведомо более сильной элюирующей способностью – растворитель Б (ацетонитрил). Растворитель А обеспечивает преимущественно транспортную функцию для перемещения в колонке уже десорбированных веществ, растворитель Б может вытеснять аналиты из сорбента в объем элюента и уменьшать времена удерживания искомых веществ. В начале разделения используется слабый элюент, но, как только из колонки вышли наиболее слабо сорбирующиеся компоненты, концентрация ацетонитрила плавно повышается, чтобы вымыть из колонки наиболее прочно удерживаемые вещества. Каждый компонент смеси, таким образом, хроматографируется при наиболее оптимальном составе элюента, что обеспечивает их полное и качественное разделение, что позволяет анализировать вещества с различной гидрофобностью. Присутствие в подвижной фазе кислоты хлорной обеспечивает удерживание органических кислот, а высокая концентрация перхлотат-иона способствует удерживанию и улучшает форму пиков соединений основного характера.
Условия хроматографирования прегабалина по условиям Базы данных «БД-2003»: подвижная фаза – А: [4M LiClO4 – 0.1M HClO4]: H2O (5:95); Б: ацетонитрил CH3CN; скорость потока подвижной фазы – 100 мкл/мин; режим - градиентный; детектирование – 210 нм; температура колонки – 40 оС; идентификация – время удерживания, спектр поглощения (рис. 1).
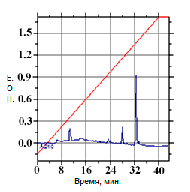
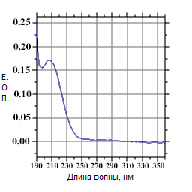
Рис. 1. ВЭЖХ-хроматограмма прегабалина (условия БД-2003) и спектр поглощения прегабалина
Время удерживания для прегабалина в данных условия в среднем составило 10,78 мин. Однако, анализирование прегабалина даже в значительной концентрации (1,5 мг/мл) не позволяет получить удовлетворительного отклика от детектора, кроме того, алифатическая природа вещества, отсутствие в структуре прегабалина большого числа хромофорных группировок не способствует повышению чувствительности в условиях УФ-детектирования.
3.3. Хроматографирование прегабалина с дериватизирующим агентом
3.3.1 Анализ в условиях «БД-2003»
Для увеличения чувствительности ВЭЖХ-анализа нами был использован прием переведения прегабалина в соединение, обладающее большим светопоглощением в УФ-области спектра.
Реакцию с прегабалином проводили с раствором дансилхлорида в среде боратного буферного раствора с рН 9,6, в течение 40-50 минут при комнатной температуре в затемненном месте, химизм взаимодействия представлен на рисунке 2. В аналогичных условиях готовили контрольную пробу (без добавления раствора прегабалина).
Хроматографирование вели по условиям «БД-2003», детектирование – при длине волны 220 нм. Наблюдали разделение производного прегабалин-дансилхлорид и дансилхлорида (рис. 3). Время удерживания производного прегабалин-дансилхлорид составило 22,99 мин, дансилхлорида – 3,48 мин.
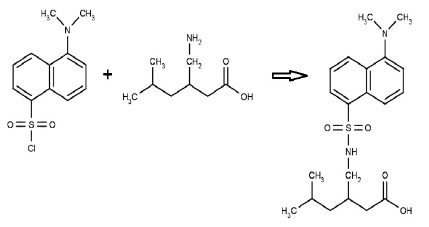
Рис. 2. Химизм реакции взаимодействия прегабалина с дансилхлоридом
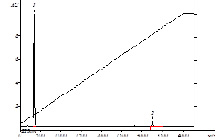
А
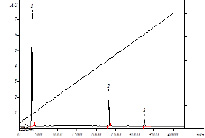
Б
Рис. 3. ВЭЖХ-хроматограмма: А – дансилхлорид,
Б – прегабалин после переведения в дансильное производное
Однако анализ в условиях «БД-2003» составляет довольно значительное время (более 40 мин.), кроме того, использование буферного раствора, в составе которого лития перхлорат и хлорная кислота, ведет к ухудшению состояния определенных частей прибора (колонка хроматографическая, термостат колонки, инжектор и др.). Поэтому далее исследования проводили с другими буферными растворами (раствор трифторуксусной кислоты 0,1% рН 2-3).
3.3.2. Анализ прегабалина с раствором трифторуксусной кислоты 0,1%
В следующих исследованиях нами применена хроматографическая система состава ацетонитрил: раствор трифторуксусной кислоты 0,1% рН 2-3 в различных соотношениях в изократическом и градиентном режиме (табл. 1).
Получить удовлетворительные параметры удерживания и симметричные формы пиков анализируемого соединения позволяет использование ацетонитрила в довольно высоких концентрациях, а также варьирование скорости потока элюента (Рис. 4, 5).
Результаты проведенных исследований по подбору оптимальных условий анализа исследуемого вещества методом ВЭЖХ могут использоваться для фармацевтических и токсикологических целей, стать основой для разработки методик качественного и количественного определения прегабалина в различных объектах исследования.
Таблица 1
Параметры удерживания прегабалина
|
№ опыта |
Условия хроматографирования |
Время удерживания, мин. |
|||||||
|
Концентрация ацетонитрила в системе, %. |
Скорость потока элюента, мкл/мин. |
Объем элюента, мкл. |
Прегабалин-дансилхлорид (пик 2) |
Дансилхлорид (пик 1) |
|||||
|
Градиентный режим |
|||||||||
|
1 |
5-80 |
100 |
2000 |
15,25 |
2,62 |
||||
|
2 |
5-90 |
100 |
2000 |
14,18 |
3,50 |
||||
|
3 |
5-100 |
100 |
2000 |
13,36 |
3,65 |
||||
|
4 |
5-100 |
150 |
2000 |
8,91 |
2,76 |
||||
|
Изократический режим |
|||||||||
|
5 |
50 |
150 |
2000 |
2,89 |
1,10 |
||||
|
6 |
50 |
100 |
2000 |
3,94 |
1,56 |
||||
|
7 |
40 |
100 |
1000 |
4,76 |
1,57 |
||||
|
8 |
60 |
100 |
1000 |
4,16 |
1,64 |
||||
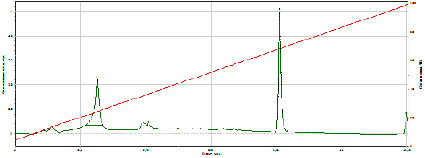
Рис. 4. Хроматографирование прегабалина в условиях опыта № 4
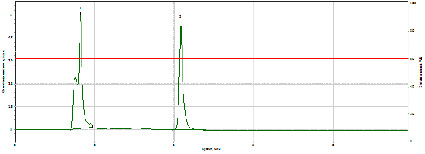
Рис. 5. Хроматографирование прегабалина в условиях опыта № 8
3.4. Получение градуировочной зависимости величины хроматографических параметров (площадь, высота) прегабалина (дансильного производного) от его концентрации в растворе
Под градуировочной зависимостью (линейностью методики) понимается наличие функциональной зависимости аналитического сигнала от концентрации определяемого вещества в анализируемой пробе. Для определения линейности нами были приготовлены растворы с концентрацией прегабалина 0,25–1,5 мг/мл, на каждом из 5-и уровней концентрации исследовали не менее 4 параллелей. Пробы анализировали в изократическом режиме с использованием хроматографической системы; раствор ТФУ 0,1% (рН 2-3): ацетонитрил (60%). В ходе исследований определяли высоту и площадь хроматографических пиков прегабалина (дансильного производного). Полученные результаты приведены в таблице 2.
Таблица 2
Результаты определения линейности ВЭЖХ-методики
|
№ опыта |
Концентрация ПДХ*, мг/мл |
Высота пика ПДХ* |
Высота ПДХ*, среднее |
Площадь пика ПДХ* |
Площадь ПДХ*, среднее |
|
1 |
1,50 |
4,38 |
4,34 |
0,72 |
0,69 |
|
2 |
1,50 |
4,31 |
0,70 |
||
|
3 |
1,50 |
4,38 |
0,69 |
||
|
4 |
1,50 |
4,30 |
0,66 |
||
|
5 |
1,00 |
3,12 |
2,96 |
0,44 |
0,44 |
|
6 |
1,00 |
2,99 |
0,44 |
||
|
7 |
1,00 |
2,89 |
0,44 |
||
|
8 |
1,00 |
2,84 |
0,43 |
||
|
9 |
0,75 |
2,12 |
2,09 |
0,32 |
0,32 |
|
10 |
0,75 |
2,12 |
0,33 |
||
|
11 |
0,75 |
2,07 |
0,31 |
||
|
12 |
0,75 |
2,06 |
0,30 |
||
|
13 |
0,50 |
1,34 |
1,32 |
0,21 |
0,22 |
|
14 |
0,50 |
1,32 |
0,22 |
||
|
15 |
0,50 |
1,31 |
0,23 |
||
|
16 |
0,50 |
1,31 |
0,22 |
||
|
17 |
0,25 |
0,63 |
0,58 |
0,11 |
0,09 |
|
18 |
0,25 |
0,59 |
0,10 |
||
|
19 |
0,25 |
0,56 |
0,08 |
||
|
20 |
0,25 |
0,56 |
0,08 |
*- ПДХ - дансильное производное прегабалина
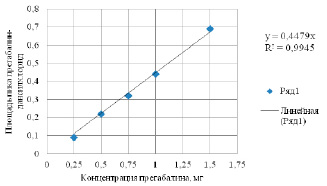
Рис. 6. Зависимость площади хроматографического пика дансильного производного прегабалина от его концентрации в растворе
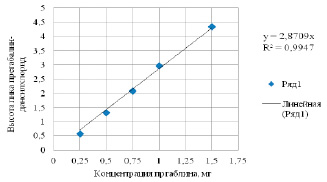
Рис. 7. Зависимость высоты хроматографического пика дансильного производного прегабалина от его концентрации в растворе
По данным строили градуировочные графики (по методу наименьших квадратов), получали корреляционные уравнения с коэффициентом корреляции 0,9945 при использовании значения площади пика и 0,9947 при использовании значения высоты пика (рис. 6, 7). Полученные уравнения зависимости площади/высоты хроматографического пика от концентрации характеризуются линейностью в диапазоне концентраций 0,25–1,5 мг/мл, и их можно использовать для определения количественного содержания прегабалина в образцах.
Заключение
1. Изучены данные литературы о лекарственном препарате прегабалин, его медицинском и немедицинском применении, методах его анализа
2. Осуществлен выбор оптимальных условий хроматографирования прегабалина методом ОФ ВЭЖХ:
- рекомендован перевод прегабалина в более светопоглощающее соединение с помощью реагента дансилхлорида;
- в качестве буферного раствора (компонент А элюента) рекомендуется применение раствора трифторуксусной кислоты 0,1% рН 2-3;
- условия анализа в изократическом режиме: концентрация ацетонитрила 60% (компонент Б), скорость потока элюента 100 мкл/мин, время удерживания прегабалин-дансилхлорид – 4,10 мин, время анализа – 10 мин.
- условия анализа в градиентном режиме: концентрация ацетонитрила с 5 до 100% (компонент Б), скорость потока элюента 150 мкл/мин, время удерживания прегабалин-дансилхлорид – 8,91 мин, время анализа – 15 мин.
3. Оценена зависимость аналитического сигнала от концентрации определяемого вещества. Методика ВЭЖХ-определения прегабалина характеризуются линейностью в диапазоне концентраций 0,25–1,5 мг/мл, коэффициенты корреляции ≥ 0,99.
Библиографическая ссылка
Хохлова Е.В. РАЗРАБОТКА МЕТОДИКИ ОПРЕДЕЛЕНИЯ ПРЕГАБАЛИНА МЕТОДОМ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ // Международный школьный научный вестник. 2018. № 5-4. ;URL: https://school-herald.ru/ru/article/view?id=729 (дата обращения: 18.01.2026).
