Последнее десятилетие такой замечательный инструмент исследователя, как зондовый сканирующий микроскоп (ЗСМ) стал более доступен. Благодаря высокому разрешению в диапазоне от микронных, до субмикронных и нано-размеров открываются широкие возможности для изучения тонкой структуры биологических объектов, не видимой в оптический микроскоп. Единственное альтернативой в нано– и субмикро-диапазоне является электронный сканирующий микроскоп ЭСМ, но он примерно в 60 раз дороже, чем ЗСМ. Единственным его преимущества по сравнению с ЗСМ является быстрота работы. Если ЗСМ строит изображение размером 100×100 мкм в приемлемом качестве за один час, то ЭСМ делает это за минуту. Однако ЗСМ позволяет не только построить контуры изображения, но определить в каждой точке другие параметры объекта, например, намагниченность, жесткость, электропроводность. При этом воздействие зонда (иглы) на объект в полу-контактном режиме не приводит к его повреждению, что особенно важно для нежных биологических объектов. Кроме того, благодаря определению локальной жесткости, можно «почувствовать» внутреннее строение биологического объекта без его препарации.
Особенно интересно использовать ЗСМ для исследования бактерий, поскольку их размер (0,5–10 мкм) меньше типичного поля зрения этого микроскопа и можно изучить одновременно десятки и тысячи бактерий. Но бактерий трудно разрезать и для изучения их строения применяют различные физико-химические методы разрушение их мембран. К сожалению, несмотря на то, что внутренние части бактерий становится видны, происходит повреждение этих частей, и исследования ведутся уже с неживыми объектами. Например, ДНК после такого воздействия образует иные объемные структуры, чем изначально в живой клетке. Только ЗСМ может подступиться к этим структурам in vivo.
Кроме того, благодаря получению дополнительных сведений о бактериях (жесткость и электропроводность мембран, размер и расположение ДНК и мезосом), ЗСМ открывает дополнительные возможности для решения задачи определения их видов и штаммов. В настоящее время существует большое число работ, посвященное изучению бактерий методом зондовой сканирующей микроскопии, в которой принимают участие целые коллективы исследователей и включающих в себя биологов и физиков.
Целью проекта является разработать и практически реализовать воспроизводимый способ параллельно расположения бактерий на подложке.
В ходе проекта решались следующие задачи:
1. Проанализировать источники литературы, касающиеся использования зондового сканирующего микроскопа (ЗСМ) для исследования бактерий.
2. Ознакомиться с теоретическими основами зондовой микроскопии и приобрести навыки работы на Наноэдюкаторе-II.
3. Провести экспериментальную апробацию предложенного способа параллельного размещения бактерий на подложке.
4. Построить распределения бактерий по углам и длинам и предложить сферы применения нашего способа.
5. Оформить лабораторную работу по нано– и биотехнологии для обучения учеников нашей школы и других школ в соответствии с программой повышения качества физического образования в Тюменской область.
Новизна работы заключается в том, что для получения статистически достоверных результатов, все бактерии в поле зрения ЗСМ должны лежать, указанным образом, т.е. быть параллельными друг другу. Поскольку определяется высота, то бактерии должны лежать на подложке без перекрытия. Этого же требует эксперименты по определению жесткостью бактерий. Анализ существующей литературы в этой области показал, что пока никто не научился располагать бактерии на подложке подобным образом [1, 2], что может сказываться на качестве получаемых результатов и достоверности выводов. Во всех изученных нами работах бактерии располагаются хаотично, а при большой поверхностной плотности – и с перекрытием.
1. Специфика работы
Спецификой работы ЗСМ в полу-контактном режиме является то, что сигнал получаемый зондом в текущей точке зависит от положения (высоты зонда) в предыдущих точках (своеобразный эффект памяти, зависящий от скорости сканирования, перепада рельефа образца и величины обратной положительной связи на зонде).
Информация, полученная о топологии исследуемого образца, сильно зависит от типа зонда и качества его изготовления. Реальный зонд не только не является идеальным точечным пробником, но не является и идеальным геометрическим телом (скажем, конусом или пирамидой). По этой причине с исследуемым образцом взаимодействуют разные части (стороны) зонда и в результате мы имеем не реальную топологию объекта, а его свертку с зондом, которая в зависимости от свойств образца (наличие шагов по высоте, глубоких и узких углублений, высокой шероховатости) может сопровождаться большим числом артефактов [4]. При этом результат сканирования может сильно зависеть от выбора угла и направления движения зонда, по отношению к образцу.
Поэтому, для получения статистически (и физически) достоверных и воспроизводимых результатов по геометрии мембран бактерий необходимо, чтобы направление сканирования зондового микроскопа было всегда под одним углом к оси бактерий, в идеале перпендикулярно ей. При хаотическом расположении бактерий, да еще и при перекрытии их друг другом получить сколь либо адекватные результаты невозможно. При сканировании одной и той же клетки под разными углами будут получены разные результаты, а о каком-то сопоставлении результатов при хаотичном расположении разных бактерий даже одного штамма и говорить не приходится.
В реальности добиться строго перпендикулярного расположения бактерий к оси сканирования невозможно и не требуется. Достаточно, чтобы этот угол был близок к 90°, и был во всех образцах одинаковым, чтобы при сканировании работали одни и те же участки зонда и полученные результаты по топологии бактерий в разных образцах были сопоставимы.
2. Методы осаждения бактерий заданным образом
Существующие методы поштучного манипулирования микро– и нано-объектами, такие как оптический пинцет [5] и зондовая нанолитография [6], в принципе позволяют располагать бактерии на подложке заданным образом. Но когда для статистической достоверности необходимы манипуляции с сотнями и тысячами бактерий, использование известных методов превратиться в кропотливую, долгую и поэтому дорогостоящую работу что проблемы фактически не решает. Теория решения изобретательских задач подсказывает, что в данном случае необходимо такое решение, в котором бактерии сами (т.е. без воздействия оператора, автоматически) располагались бы на подложке параллельно друг другу.
Нами было предложено и апробировано такое решение исходя из использования пространственно-периодических Ван дер Ваальсовых сил. Мы предлагаем использовать подложки, поверхность которых имеет на нано-уровне периодический рельеф (например, синусоидальный). При осаждении бактерий из раствора они, в первую очередь, будут касаться выступов рельефа, а затем будут притянуты к подложке по направлению вдоль этих выступов, поскольку в этом направлении действие молекулярных сил притяжения между поверхностями бактерии и подложки максимально.
В процессе такого направленного осаждения бактерий из жидкости на подложку важно уменьшить подвижность бактерий с тем, чтобы сила ее собственного смещения стала меньше Ван дер Ваальсовых сил. Это можно осуществить двумя непротиворечащими друг другу путями. Первый путь – это охладить подложку и жидкость с бактериями почти до 0°С, тем самым понизить собственную подвижность бактерий. Второй путь – осаждать бактерии при комнатной температуре, но внести в раствор водорастворимую компоненту, не оказывающую негативного воздействия на бактерию (это может быть сахар или другая питательная субстанция), но существенно повышающую вязкость раствора. В этом случае движение и изгиб бактерий будет значительно подавлен силами вязкого трения в растворе.
3. Экспериментальная апробация
В наших экспериментах подложками для осаждения бактерий служили покровные стекла 18×18×0,018 мм, у которых с помощью ЗСМ Наноэдюкатор-2 (Зеленоград НТ-МДТ), работающего в полу-контактном режиме, был обнаружен синусоидальный рельеф с пространственным периодом 4 нм и высотой 3–4 нм, который возник, по-видимому, в процессе их изготовления, рис. 1.
В качестве бактерий использовали штамм Bifidobacterium Longum MC-42, а в качестве вязкого раствора для осаждения – исходный (не разбавленный) раствор жидкого пробиотика «Биовестин».
3.1. Процесс приготовления препарата
Покровные стекла обезжиривали 96 % этанолом медицинским (ООО СБИО, серия 30316). Затем стекла высушивали и помещали их по одному на дно стерильных пластиковых чашек Петри с крышкой диаметром 60 мм (Медполимер, СПб). Выливали в каждую чашку по одному флакону Биовестина, предварительно вынутому из холодильника и принявшему комнатную температуру. Закрывали чашки крышками и выдерживали раствор для осаждения бактерий в течение 20 минут. Затем промывали стекла дистиллированной водой, помещали их в новые чашки Петри, закрывали крышкой и оставляли их на сутки для высыхания.
3.2. Процесс сканирования
Образцы прикрепляли на столик ЗСМ Наноэдюкатор-2 с помощью двухстороннего скотча и осуществляли их сканирование в полу-контатном режиме на воздухе в масштабе 100×100 мкм и ниже при частоте сканирования 0,07 Гц на линию, что при разрешении снимка 256×256 пикселей давало время сканирования 1 час. Рабочая точка обратной связи была установлена в 8 нА, как 80 % от максимальной амплитуды колебаний зонда, а коэффициент обратной связи был выбран равным 0,4. Направления сканирования было выбрано слева направо. Более медленное сканирование не добавляло качества изображению, а более быстрое приводило к появлению артефактов в виде вытягивания правых краев бактерий вследствие медленной работы обратной связи вертикального положения зонда. Увеличение же усиления обратной связи приводило к самовозбуждению зонда на резонансной частоте и появлению муара на изображении. В качестве зонда служила вольфрамовая проволочка диметром 300 мкм, заостренная путем отрезания.
3.3. Результат сканирования
На всех образцах было получено параллельно расположение бактерий в поле зрения, рис. 1, соответствующее предварительно установленному параллельному расположению периодичности их рельефа, рис. 1. При этом, случаи перекрывания бактерий друг другом (когда одна бактерия лежала прямо на другой) носили единичный характер и могли быть практически полностью устранены уменьшением времени осаждения бактерий.
Тот факт, что большинство бактерий лежало на подложке, не перекрываясь друг с другом, связан с тем, что сила притяжения молекул мембраны бактерии к молекулам подложки из силикатного стекла существенно выше силы притяжения молекул мембран двух бактерий. Поэтому, если данное место подложки уже занято осевшей бактерией, то силы притяжения к этой бактерии другой бактерии, как правило, недостаточно для прикрепления последней. За счет подвижности второй бактерии (например, ее броуновского движения) она перемещается дальше, пока не коснется пустого участка подложки. В этом случае сила притяжения между мембраной и подложкой уже достаточна, чтобы прикрепить бактерию к подложке.
Только в случае, если на заданном участке подложки уже имеется сплошной слой прикрепившихся бактерий и доступ к подложке отсутствует, а раствор с бактериями еще находится на подложке, будет происходить прикрепление бактерий вторым слоем поверх первого, причем так, что параллельность расположения бактерий сохраняется. Это связано с тем, что сила притяжения бактерий друг к другу гораздо слабее, чем бактерий к подложке, и поэтому прикрепление бактерий возможно, если только одна бактерия коснулась другой, будучи параллельной и почти точно расположенной над ней (почти без сдвига вдоль оси). При непараллельном касании или параллельном касании без перекрытия осаждаемая бактерия в состоянии оторваться от уже прикрепленной на подложку. Эти рассуждения хорошо подтверждаются результатами сканирования, на которых видно, что прикрепляемые вторым слоем бактерии садятся на бактерии первого слоя практически точно одна на другую, рис. 1.
3.4. Оценка степени параллельности
Для оценки степени параллельности расположения бактерий на подложке измеряли координаты противоположных точек вдоль длинной оси бактерий на изображениях образцов в программе Microsoft Paint 6, а затем в программе Microsoft Office Excel 2003 по этим данным рассчитывали углы поворота бактерий относительно оси абсцисс изображения.
Результаты измерений по 300 бактериям образца, показанного на рис. 2, приведены на рис. 3. Установили, что 90 % бактерий имеют угол, отличающийся от среднего не более чем на ± 4°, а 95 % – не более чем на ± 5°.
Это более чем достаточно, чтобы устранить влияние разного направления сканирования зонда по отношению к оси бактерий на результаты определения их геометрических размеров.
Важно отметить и негауссов характер распределения бактерий по углам (провал на 31° и пики на 30° и 33°), который говорит о том, что отклонение бактерий от среднего угла 31° не полностью случайно, а подчиняется некой закономерности. Данная закономерность, очевидно, связана с пространственной немонотонностью угла периодической структуры подложки. Мы использовали покровное стекло, у которого данный рельеф возник в процессе его изготовления. В дальнейшем планируем использовать в качестве подложек нарезные стеклянные и металлические дифракционные решетки, структура поверхности которых четко определена. Однако предстоит еще выяснить, как будет влиять большая глубина рельефа решеток, сопоставимая с диаметром бактерий на их расположение на подложке.
Чтобы убедиться, что угол положения бактерий сохраняется и за пределами небольшого поля зрения (максимум 100×100 мкм) сканирующего микроскопа, были просканированы 9 областей на одной подложке, центры которых были расположены в шахматном порядке и удалены по осям абсцисс и ординат на 2,5 мм друг от друга, рис. 3. Для этого, образец с бактериями, осажденными нашим методом, помещался на столик микроскопа при нулевом выведении его микрометрических винтов. Сканировали область подложки 20×20 мкм с частотой 0,15 Гц на линию, что соответствовало времени сканирования области 30 минут. Все остальные настройки ЗСМ были теми же, что указаны выше. Затем смещали образец строго параллельно микрометрическими винтами микроскопа по одной и / или двум осям с шагом 0 и ± 2,5 мм (полный ход микрометров был равен 5 мм).
Средние углы положения бактерий и доверительный интервал при доверительной вероятности 0,95 на 9 участках одной подложки
|
Отсчеты микрометров микроскопа по двум осям, мм |
Угол, град |
||
|
– 2,5 |
0 |
+ 2,5 |
|
|
– 2,5 |
34,8 ± 1,7 |
34,4 ± 1,2 |
33,3 ± 1,3 |
|
0 |
32,4 ± 1,1 |
36,0 ± 1,5 |
31,3 ± 1,2 |
|
+ 2,5 |
32,8 ± 1,0 |
37,6 ± 1,4 |
37,1 ± 0,9 |
Результаты, приведенные в таблице, показывают, что параллельность расположения бактерий сохраняется на области подложки 5´5 мм в пределах ошибки ± 3,2° от среднего значения в 34,41° по всем площадкам. Усреднение угла производили по 30–50 бактериям в поле зрения. При этом, хотя средние углы положения бактерий на 9 исследованных площадках близки, распределение углов является немонотонным и объясняется немонотонностью угла периодического рельефа подложки, что было отмечено еще при анализе рис. 3.
Заключение
1. В ходе выполнения работы был разработан способ параллельного расположения бактерий на твердые подложки. Экспериментальные исследования с зондовым сканирующим микроскопом показали, что 90 % бактерий имеют угол, отличающийся от среднего не более чем на ± 4 °, а 95 % – не более чем на ± 5 °.
2. Получены два свидетельства о государственной регистрации программ для ЭВМ: № 2017661512 «Определение длин бактерий по их изображениям в зондовый сканирующий микроскоп» и № 2017661513 «Определение углов расположения бактерий на подложке по отношению к направлению сканирования зондового микроскопа».
3. Готовятся заявка на изобретение «Способ параллельного расположения бактерий на подложки» и статья в реферативный журнал «Биотехнология» в раздел «Технология биопрепаратов».
4. Готовится методичка по лабораторной работе, демонстрирующий наш способ, для учащихся Физико-математической школы Тюменской области и студентов Тюменского госуниверситета направлений «Нанотехнологии» и «Биология».
Приложение


Рис.1 Бактерии на покровном стекле в 2D и 3D. Масштаб 100×72 мкм
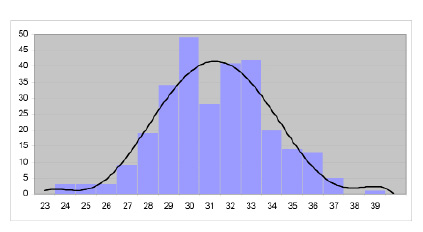
Распределение бактерий (штук) по углу (град.)
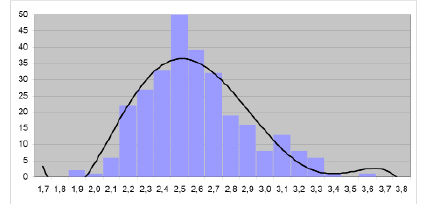
Распределение бактерий (штук) по длине (мкм)
Рис.2. Результаты по геометрии и расположению бактерий на подложке

Рис. 3. Бактерии на покровном стекле в 2D. Масштаб 20×20 мкм
Библиографическая ссылка
Банков А.А. МЕТОД ПАРАЛЛЕЛЬНОГО РАСПОЛОЖЕНИЯ БАКТЕРИЙ НА ПОДЛОЖКЕ ДЛЯ ПОВЫШЕНИЯ ТОЧНОСТИ ИХ ИССЛЕДОВАНИЯ МЕТОДАМИ ЗОНДОВОЙ СКАНИРУЮЩЕЙ МИКРОСКОПИИ // Международный школьный научный вестник. 2019. № 1-1. ;URL: https://school-herald.ru/ru/article/view?id=850 (дата обращения: 15.02.2026).
