Данная статья является реферативным изложением основной работы. Полный текст научной работы, приложения, иллюстрации и иные дополнительные материалы доступны на сайте VI Международного конкурса научно-исследовательских и творческих работ учащихся «Старт в науке» по ссылке: https://school-science.ru/6/13/37559.
Первая повесть о Шерлоке Холмсе и докторе Ватсоне, автором которой является Артур Конан Дойл, появилась на свет в 1887 г. С «Этюда в багровых тонах» началась эра бесконечных приключений великого сыщика и его друга, вдохновивших и других авторов на написание новых историй [6].
Из рассказов о Холмсе мы знаем, что тот обладал обширными знаниями по химии. Еще обучаясь в колледже, он около двух месяцев занимался в Лондоне опытами по органической химии, и даже некоторое время работал лаборантом в одной из лондонских больниц. Будущий сыщик постоянно проводит рискованные химические эксперименты в своей квартире, нередко наполняя её удушливыми парами [5].
И все же Шерлок Холмс был не просто любителем химии. Он на самом деле испытывал страсть к точным и достоверным знаниям. По этой причине в произведениях о нем особое внимание уделяется химической науке – органической, неорганической, аналитической [6].
Два сотрудника университета штата Теннесси (США) Т.Г. Уоддел и Т.Р. Райболт сочинили серию новых рассказов о расследованиях великого детектива, которые были опубликованы в журнале «JournalofChemicalEducation». При прочтении этих криминальных историй и погружении в детали преступлений, возникает вопрос: верны ли описанные события, с научной точки зрения, или это художественный вымысел [4]?
Цель работы: изучить некоторые рассказы Т.Г. Уоддела и Т.Р. Райболта о химических приключениях Шерлока Холмса и выяснить, какие признаки, и свойства веществ они отразили в своих произведениях.
Объекты исследования: рассказы «Дело о стехиометрическом решении», «Проблема Вултонской тюрьмы», «Побег из тюрьмы Блэкуотер».
Гипотеза: описанные в рассказах свойства веществ и их превращения правильны с научной точки зрения.
Задачи исследования:
1. Опираясь на детали рассказа «Дело о стехиометрическом решении», выяснить, возможно ли совершить преступление описанным способом, и рассчитать необходимые для этого количества углекислого газа и уксусной кислоты.
2. Изучив произведение «Загадка Вултонской тюрьмы», проверить, возможно ли передать сообщение, используя крахмал в качестве симпатических чернил.
3.Установить, можно ли используя процесс электролиза, о котором идет речь в рассказе «Побег из тюрьмы Блэкуотер», отогнуть стальную решетку на окне.
1. Литературный обзор
1.1. Влияние оксида углерода (IV) на здоровье человека
Углекислый газ (угольный ангидрид, двуокись углерода) – бесцветный газ с кисловатым запахом и вкусом. Он почти в 1,5 раза тяжелее воздуха. В атмосферном воздухе углекислый газ содержится в виде примеси и пополняется в основном за счет активности вулканов, жизнедеятельности микроорганизмов почвы и сжигания топлива. Относительное постоянство содержания СО2 в атмосферном воздухе поддерживается благодаря поглощению его Мировым океаном и усвоению растительным миром. Однако концентрация углекислого газа в атмосфере Земли повышается в связи с деятельностью человека [2].
Влияние CO2 на организм
Различные исследования по влиянию CO2 на организм человека были проведены ещё в прошлом веке. В 60-ых годах учёная О. В. Елисеева приводит детальное исследование, как влияет углекислый газ в концентрациях от 0,1 % (1000 ррm) до 0,5 % (5000 ррm) на организм человека, и пришла к выводу, что кратковременное вдыхание здоровыми людьми двуокиси углерода в этих концентрациях вызывает изменения в функции внешнего дыхания, кровообращении и ухудшения электрической активности головного мозга. Согласно ее рекомендациям, содержание CO2 в воздухе жилых и общественных зданий не должно превышать 0,1 % (1000 ррm), а среднее содержание CO2 должно быть около 0,05 % (500 ррm) (приложение 1) [1].
Существует непосредственная взаимосвязь между концентрацией CO2 и самочувствием человека. На уровне 0,08 % (800 ррm) уже возникает ощущение духоты, а больной человек еще более восприимчив. А в современных офисах концентрация углекислого газа может превышать рекомендации в 4 раза (Приложение 2).
Когда у человека высокий уровень углекислого газа в крови, наступает состояние, известное как гиперкапния. Оно может вызвать покраснение кожи, повышение артериального давления, судороги, снижение мозговой и нервной активности, головные боли, спутанность сознания и сонливость. В крайнем случае, человеку для восстановления нормального дыхания будет необходима кислородная маска. Длительная гиперкапния может привести к повреждению внутренних органов, и даже мозга.
Низкий уровень углекислого газа в крови также может быть очень вредным для организма. Показатели СО2 снижаются из-за учащенного дыхания, в результате которого в организм поступает больше кислорода, чем нужно.
Диоксид углерода повышает кислотность крови, потому что образует слабую угольную кислоту (CO2 + Н2O = Н2СО3), распадающуюся на Н+ и НСО3–А когда его уровень низок, кровь ощелачивается, что приводит к сужению кровеносных сосудов и ухудшению кровотока. Это может быть очень опасным, поскольку приводит к снижению кровоснабжения мозга, а, следовательно, к помутнению сознания, головокружению, ухудшению зрения, мышечным судорогам и беспричинной тревожности. [13] (Приложение 2)
Чертовы места
Каждый из живущих вблизи Неаполя хоть раз слышал о Собачьей пещере (GrottadelCane. Слава пещеры построена на костях собак, принадлежащих слишком любопытным владельцам. Человек мог беспрепятственно войти в неё и выйти, а его четвероногий спутник – нет. И чем дольше животное находилось в пещере, тем больше был шанс, что оно погибнет. В XX веке люди поговаривали о злых духах, скрывающихся от солнечного света во мраке подземелья, что душили собак. Собаки и правда были задушены, но не нечистой силой, а природной аномалией. На сегодняшний день известно, что Собачья пещера вырабатывает углекислый газ, который скапливается в 80см над землёй. Голова человека находится в воздушном слое, а голова собаки в атмосфере смертоносного газа. Но животное погибает не сразу. Сначала замедляются реакции, потом происходит потеря сознания, и если собаку оперативно не поднять, а лучше вынести на свежий воздух, то она погибнет. Из-за череды дурных событий злополучная пещера является популярным объектом среди туристов. Но многие забывают, что она опасна не только для собак, но и для человека, который, к примеру, присел, чтобы завязать себе шнурки или сделать несколько удачных кадров... В зависимости от состояния здоровья, некоторые могут расстаться с жизнью быстрее, чем планировали. Именно поэтому не рекомендуется посещение этого места в одиночку [7].
В районах с высокой сейсмической активностью, сопровождающейся разломами земной коры, активизацией вулканов и гейзеров, могут образовываться, как их называет местное население, «чертовы места», «мертвые долины», «чертовы кладбища» и так далее. Обычно – это естественные замкнутые впадины рельефа, которые отличаются от окружающего ландшафта разными признаками, зависимо от того, какие вещества концентрируются в этом месте. Сероводород, например, убивает растительность и окрашивает все в желто-коричнево-бурые тона.
Но есть места, наоборот, отличающиеся обильной растительностью. Размеры растений в таких местах значительно превышают размеры представителей флоры в других местах. Это связано с тем, что на дне этих непродуваемых ветром впадин накапливается углекислый газ, который в 1,5 раза тяжелее воздуха, стимулирующий усиленный рост растительности. Здесь можно наблюдать большое количество скелетов и трупов представителей местной фауны – буйная растительность привлекает мелких животных, но не чувствуя угрозы жизни, выйти обратно уже не успевают. Известны редкие случаи гибели в таких местах людей. Чаще всего – это пришлые люди. Местное население обычно очень хорошо знает такие места и старается обходить их стороной. [7]
Смертельные случаи отравления углекислым газом
В практике судебно-медицинских экспертов редко, но наблюдаются случаи отравления углекислым газом.
Первый случай. Двое рабочих обследовали канализационные колодцы. Один из рабочих, спускаясь в колодец, потерял сознание в 1,5 м от земли и упал на дно колодца. Второй рабочий стал спускаться с целью его извлечения, почувствовал себя плохо и с трудом поднялся. Через 40 минут прибыли спасатели, спустились в колодец в противогазах, извлекли пострадавшего, но он уже был мертв. Исследования проб воздуха показали, что содержание углекислого газа в воздухе на дне колодца составляло 9 %, кислорода 8,6 %.
Второй случай. Слесарь при производстве работ без мер предосторожности, без веревки стал спускаться в люк канализационного колодца и упал на дно его. Затем три человека, пытаясь его спасти также потеряли сознание и упали. Слесарь умер, остальные были отправлены в больницу и выписались через день в удовлетворительном состоянии. Исследования показали, что на глубине 4,5 м содержание СО2 было 8,7 %, кислорода – 5,4 %.
При исследовании погибших было установлено, что кожа лица посинела, полости сердца и крупные сосуды заполнены жидкой темной кровью, наблюдались многочисленные точечные кровоизлияния.
Анализ сведений и дополнительных исследований показал, что смерть обоих пострадавших наступила в результате отравления углекислым газом.
Поэтому при спуске людей в колодцы, силосные башни, погреба и овощехранилища необходимо строго соблюдать правила техники безопасности. Медицинские работники в профилактических целях должны информировать население о потенциальной опасности, периодически контролировать концентрации углекислого газа в различных помещениях такого типа, рекомендовать установку в них вентиляции [11].
Невидимые (симпатические) чернила – это чернила, записи которыми являются изначально невидимыми и становятся видимыми только при определенных условиях (нагрев, химический проявитель, ультрафиолетовые или инфракрасные лучи и др.).
В зависимости от характера взаимодействия веществ, все невидимые (симпатические) чернила можно условно разделить на такие виды:
• химические;
• фоточувствительные;
• люминесцентные;
• термочувствительные;
• влагочувствительные [9].
Химические чернила
В состав химических чернил входят бесцветные или слабо окрашенные вещества, которые при реакции образуют ярко окрашенные продукты. Раствор «чернил» наносится на бумагу и высушивается при комнатной температуре. Изображение обнаруживается раствором проявителя или его называют электролит, при помощи пульверизатора или ватного тампона. Иногда проявитель представляет собой газообразное вещество.
Химическими чернилами пользовались немецкие шпионы. В 1915 году из Англии в Норвегию шпионом было отправлено письмо с важным документом. На первый взгляд, это была нотная тетрадь. Между строчек нотной тетради немецкий агент сделал надписи с помощью симпатических чернил. Британская контрразведка смогла проявить эту тайнопись, что привело к разоблачению германского шпиона. В состав чернил входил гексацианоферрат калия, текст стал видимым после обработки бумаги солями железа.
Фоточувствительные чернила
Фоточувствительными называются чернила, способные проявляться или исчезать под действием света.
Первая группа таких чернил содержит бесцветные или слабоокрашенные вещества, которые разлагаются при освещении видимым светом. Продукты разложения таких веществ окрашены или образуют окрашенные соединения в результате взаимодействия с другими компонентами чернил. Ко второй группе относятся чернила, «исчезающие» при освещении и снова проявляющиеся в темноте. Фоточувствительные чернила наносят на бумагу и высушивают на воздухе. Надпись проявляют или удаляют, освещая ее ярким солнечным светом.
Люминесцентные чернила
Эта группа чернил содержит бесцветные либо слабо окрашенные вещества, способные к люминесценции под действием ультрафиолетового излучения. Для проявления таких чернил надпись освещают ультрафиолетовой лампой. После прекращения действия ультрафиолета надпись исчезает. Люминесцентные чернила активно используются полицией и спецслужбами, а также студентами – во время контрольных или экзаменов.
Термочувствительные чернила
В состав термочувствительных симпатических чернил входят бесцветные или слабо окрашенные вещества, которые переходят в окрашенные соединения при нагревании. Во многих случаях окраска появляется в результате взаимодействия компонентов чернил с бумагой. Чернила наносятся на бумагу и высушиваются при комнатной температуре. Тайнопись или рисунок проявляется при нагревании до 120–180°С (можно прогладить горячим утюгом, подержать ее над пламенем или сильно нагретой электроплиткой).
В зависимости от характера химического воздействия на бумагу при проявлении скрытого изображения, термочувствительные чернила делятся на 3 группы:
Дегидратирующие чернила. Это - разбавленные (2–10 %) водные растворы серной или фосфорной кислот, гидросульфата натрия. При нагревании эти вещества обезвоживаются и оказывают на бумагу сильное дегидратирующее (обезвоживающее) действие. В результате бумага в местах нанесения чернил частично обугливается и появляется надпись, окрашивается в цвета от светло-коричневого до черного.
Окисляющие чернила. В их состав входят вещества, способные при нагревании до 150–180°С окислять материал бумаги, восстанавливаясь при этом с образованием окрашенных соединений. К таким чернилам относятся разбавленные (1–5 %) водные растворы метаванадата аммония и парамолибдата аммония, реактив Толленса. При нагревании метаванадат аммония восстанавливается бумагой с образованием смеси оксидов ванадия, окрашенной в цвета от коричневого до черного. Парамолибдат аммония образует «молибденовую синь», а реактив Толленса - мелкодисперсное серебро чёрного цвета.
Нейтральные чернила. При проявлении скрытого изображения они не оказывают химического воздействия на бумагу, а лишь окрашивают ее продуктами своего разложения. К таким чернилам относятся, например, соки лимона, репчатого лука, яблок, а также молоко и сыворотка крови. Органические вещества, входящие в их состав (кислоты, белки, углеводы и другие) при нагревании до 150–180°С разлагаются с образованием продуктов, окрашенных в цвета от желтого до светло-коричневого.
Влагочувствительные чернила
Невидимые надписи или изображения, сделанные влагочувствительными чернилами, проявляются водой или водяным паром. В зависимости от характера процессов проявления такие чернила делятся на две группы:
Просвечивающие чернила. Надписи, сделанные ими, после высыхания на бумаге совершенно незаметны, но проявляются при выдерживании ее в воде в течение 2 – 3 минут. Участки бумаги, пропитанные этими чернилами, становятся под действием воды полупрозрачными. При высыхании бумаги надпись исчезает. К таким чернилам относится «раствор Видемана». Он готовится путем интенсивного смешивания льняного масла, 25 %-ного раствора аммиака и воды в объемном соотношении 1:20:100. В состав таких чернил вместо льняного масла могут входить и некоторые другие масла растительного происхождения.
Клеящие чернила. Изображения или надписи, сделанные ими, проявляются водяным паром с последующей обработкой порошком пигмента. Для проявления бумагу с невидимой надписью держат над водяным паром (100°С) в течение 5 секунд, не допуская ее переувлажнения и образования на ней капелек воды. Затем, держа бумагу вертикально, посыпают ее очень мелким порошком какого-нибудь окрашенного вещества. Избыток порошка удаляют стряхиванием. Участки бумаги, пропитанные указанными чернилами, после обработки паром становятся липкими и за счет этого удерживают частицы пигмента – надпись «проявляется». В качестве таких чернил можно использовать водные растворы сахарозы, глюкозы и других углеводов (5-15 %), нагретые растворы желатина (1-3 %), растворов столярного клея (1–3 %) и других клеящих веществ. [9]
История секретных чернил. Ещё в I веке н. э. Филон Александрийский описал рецепт симпатических чернил из сока чернильных орешков, для проявления которых требовался раствор железомедной соли. Овидий предлагал использовать молоко в качестве невидимых чернил (проявляется после нагрева).
Тайные агенты Ивана Грозного писали свои донесения луковым соком. Буквы становились видимыми при нагревании бумаги. Ленин использовал для тайнописи сок лимона или молоко. Для проявления письма в этих случаях достаточно прогладить бумагу горячим утюгом или подержать ее несколько минут над огнем.
Знаменитая шпионка Мата Хари тоже использовала секретные чернила. Когда она была арестована в Париже, в ее гостиничном номере нашли пузырек с водным раствором хлорида кобальта, что и стало одной из улик при разоблачении ее шпионской деятельности. Хлорид кобальта можно успешно использовать для тайнописи: буквы, написанные его раствором, содержащим в 25 мл воды 1 г соли, совершенно невидимы и проявляются, делаясь синими, при легком нагревании бумаги.
Секретные чернила широко применялись и в России революционерами-подпольщиками. В 1878 году Вера Засулич смогла сбежать из-под ареста, сообщив заранее своим друзьям о плане побега с запиской с просьбой принести кое-что из одежды,которая содержала на обратной стороне листка информацию, написанную водным раствором хлорида железа FeCl3 (Засулич принимала это вещество как лекарство). Такую записку можно прочесть, обработав ее ватным тампоном, смоченным разбавленным водным раствором тиоцианата калия: все невидимые буквы станут кроваво-красными из-за образования тиоцианатного комплекса железа.
Члены тайной организации «Черный передел» тоже использовали в переписке невидимые чернила – разбавленный водный раствор медного купороса. Проявлялся написанный такими чернилами текст, если бумагу подержать над склянкой с нашатырным спиртом. Буквы окрашиваются в ярко-синий цвет из-за образования аммиачного комплекса меди.
А вот китайский император Цин Шихуанди (249-206 гг. до н. э.), во время правления которого появилась Великая Китайская стена, использовал для своих тайных писем густой рисовый отвар, который после высыхания не оставляет никаких видимых следов. Если такое письмо слегка смочить слабым спиртовым раствором йода, то появляются синие буквы. А император для проявления письма пользовался бурым отваром морских водорослей.
Еще один рецепт секретных чернил включает применение 10 %-го водного раствора желтой кровяной соли. Написанные этим раствором буквы исчезают при высыхании бумаги. Чтобы увидеть надпись, надо смочить бумагу 40 %-м раствором хлорида железа. Ярко-синие буквы, которые появляются при такой обработке, уже не исчезают при высыхании. Появление букв связано с образованием комплексного соединения, известного под названием «турнбулева синь» [9].
Поэтому в качестве симпатических чернил могут быть использованы самые различные вещества (приложение 3).
Электролиз – это окислительно-восстановительный процесс, который происходит на электродах во время прохождения электрического тока через расплав или раствор.
Для проведения электролиза нужен источник тока, два электрода и, конечно, электролит. Электролит – это раствор, который проводит электрический ток.
Различают электролиз растворов и электролиз расплавов. Оба эти процесса существенно отличаются друг от друга. Отличие – в наличии растворителя. При электролизе растворов кроме ионов самого вещества в процессе участвуют ионы растворителя. При электролизе расплавов – только ионы самого вещества.
Для того чтобы получить нужный продукт (газ, металл или неметалл), нужно правильно выбрать электрод и раствор электролита.
Электродами могут служить любые материалы, проводящие электрический ток. В основном применяют металлы и сплавы, из неметаллов электродами могут служить, например, графитовые стержни (или углерод). Реже в качестве электрода используют жидкости [8].
Электрод, заряженный положительно – анод. Электрод, заряженный отрицательно – катод. При электролизе происходит окисление анода (он растворяется) и восстановление катода. Именно поэтому анод следует брать таким, чтобы его растворение не повлияло на химический процесс, протекающий в растворе или расплаве. Такой анод называют инертным электродом. В качестве инертного анода можно взять графит (углерод) или платину. В качестве катода можно взять металлическую пластину (она не будет растворяться): медь, латунь, углерод (или графит), цинк, железо, алюминий. Электролиз с растворимым (активным) анодом: если анод выполнен из металла с потенциалом более низким, чем потенциалы окисления других частиц, присутствующих в данной системе, то происходит анодное растворение и катодное осаждение одного и того же металла. Например, на медных электродах – на аноде окисляется медь:
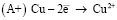 .
.
По мере образования ионов меди на аноде и их накопления в прикатодном пространстве на катоде начнут восстанавливаться ионы меди: 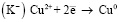 (приложение 4)
(приложение 4)
Электролиз широко применяется в различных отраслях промышленности. В химической промышленности электролизом получают такие важные продукты как хлор и щелочи, хлораты и перхлораты, надсерную кислоту и персульфаты, перманганат калия, органические соединения, химически чистые водород, кислород, фтор и ряд других ценных продуктов. В цветной металлургии электролиз используется для рафинирования металлов, для извлечения металлов из руд. Металлы, которые не могут быть выделены из водных растворов вследствие высокого отрицательного потенциала, получают в цветной металлургии электролизом расплавленных сред, в качестве которых служат соли этих металлов, содержащие добавки различных соединений, вводимые с целью понижения температуры плавления расплава, повышения электропроводности и т.д. К числу металлов, получаемых электролизом расплавленных сред относятся алюминий, магний, цирконий, титан, уран, бериллий и ряд других металлов.
Электролиз применяют во многих отраслях машиностроения, радиотехники, электронной, полиграфической промышленности для нанесения тонких покрытий металлов на поверхность изделий для защиты их от коррозии, придания декоративного вида, повышения износостойкости, жаростойкости, получения металлических копий.
Законы Фарадея. Работам М. Фарадея суждено было стать важнейшим звеном в цепи событий, сделавших нашим достоянием технические достижения в области электрохимии и электричества. В них отражалась количественная связь между массой вещества, выделяемого при электролизе, и необходимым для этого количеством электричества, стало возможным количественно предсказать ход определенных электрохимических процессов и экспериментально определить эквивалентные массы химических элементов. Исходя из эквивалентных масс веществ, можно рассчитать их молекулярные массы. Связав свои исследования электрических явлений с атомистическими представлениями в химии, Фарадей стал предвестником современного учения о строении атома.
В учебниках и научной литературе можно найти несколько версий формулировки законов М. Фарадея. В наиболее общем виде законы формулируются следующим образом:
Первый закон электролиза Фарадея: масса вещества, осаждённого на электроде при электролизе, прямо пропорциональна количеству электричества, переданного на этот электрод. Под количеством электричества имеется в виду электрический заряд, измеряемый, как правило, в кулонах.
Второй закон электролиза Фарадея: для данного количества электричества (электрического заряда) масса химического элемента, осаждённого на электроде, прямо пропорциональна эквивалентной массе элемента. Эквивалентной массой вещества является его молярная масса, делённая на целое число, зависящее от химической реакции, в которой участвует вещество.
Законы Фарадея можно записать в виде следующей формулы:
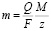 ,
,
где m – масса осаждённого на электроде вещества в граммах; Q – полный электрический заряд, прошедший через вещество; F = 96 485,33(83) Кл·моль-1 – постоянная Фарадея; M – молярная масса вещества; z – валентное число ионов вещества (число электронов на один ион).
Заметим, что M/z – это эквивалентная масса осаждённого вещества.
Для первого закона Фарадея M, F и z являются константами, так что чем больше величина Q, тем больше будет величина m.
Для второго закона Фарадея Q, F и z являются константами, так что чем больше величина M/z (эквивалентная масса), тем больше будет величина m.
В простейшем случае постоянного тока электролиза Q=It приводит к:
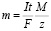
и тогда
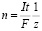 ,
,
где n – выделенное количество вещества («количество молей»): n = m/M; t – время действия постоянного тока в секундах [10].
2. Исследовательская часть
История 1. В рассказе «Дело о стехиометрическом решении» говорится о расследовании смерти человека в запертой комнате размером 7×7×8 футов в известковой каменоломне. Шерлок Холмс выясняет, что жертва задохнулась вследствие заполнения помещения углекислым газом, выделившимся при взаимодействии уксусной кислоты и известняка. [4] Углекислый газ попал в комнату через вентиляционное отверстие. Возможность использовать уксусную кислоту как реагент в реакции была у двух героев рассказа. Один из них производил уксус и растительное масло, у второго же несколько бутылок ледяной уксусной кислоты обнаружили в квартире при обыске. Кто же из них преступник? Я провела несколько опытов.
Опыт 1. Получение и обнаружение оксида углерода (IV).
Материалы и реактивы:CaCO3, растворCH3COOH, Ca(OH)2
Ход работы: добавили уксусную кислоту в известняк, в результате чего выделился газ. При пропускании газа через известковую воду выпал белый осадок. Это подтверждает, что выделившимся газом был диоксид углерода [2] (фото 1).
Углекислый газ – без цвета, без вкуса и запаха, Dвозд.= 44/29=1,5. Легко сжижается и затвердевает, образуя «сухой лед». Не поддерживает дыхание.
Расчеты по данным:
Размеры комнаты
7×7×8 футов = 392 фута3 [4]
1 фут3 = 0,0283 м3
Объем комнаты= 392 • 0,0283= 11,1 м3= =11100 л
По уравнению реакции
2 CH3COOH + CaCO3 → Ca(CH3COO)2 + +H2O + CO2↑
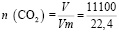 моль
моль
n(CH3COOH)=2n(CO2)=2•495,54=991,08 моль
m(CH3COOH)= n•M=991,08•60= =59465,35 г=59,465 кг.
Если использовать разбавленную 9 % уксусную кислоту, то количество необходимого раствора m р-ра= 59/0,09=656 кг.
Так как плотность уксусной кислоты примерно равна 1050 г/л, то
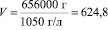 л.
л.
Глубокий след, оставленный вблизи вентиляционного отверстия, говорит о нагруженной повозке. Следовательно, производитель уксуса и масла, имеющий бочки и баки для ферментации, мог осуществить данную реакцию.
Вывод: углекислый газ действительно можно получить описанным способом. Высокая концентрация углекислого газа вызывает ухудшение состояния человека. Из дополнительной литературы выяснили, что даже в низких концентрациях углекислый газ в помещении становится токсичным, поскольку воздействует на клеточную мембрану и в крови человека происходят биохимические изменения, такие, как ацидоз (изменение кислотно-щелочного равновесия в организме) [13].
История 2. Рассказ «Загадка Вултонской тюрьмы» повествует о том, как криминальная группировка возобновила свою работу, в то время как ее глава находится в тюремном заключении. Выяснилось, что он передавал тайные послания на газетах своим подчиненным, используя при этом крахмал. Чтобы проявить надпись, по словам мистера Холмса, им нужно было лишь смочить газету раствором йода.
Опыт 2. Симпатические чернила.
Материалы и реактивы: крахмал, молоко, лимонный сок, раствор Ca(OH)2, фенолфталеин, раствор йода, электрический утюг, листы бумаги.
Ход работы: для исследования описанного в рассказе способа тайнописи мы использовали несколько видов симпатических чернил:
1. Крахмал (проявляется при обработке йодом)
2. Молоко (нагрев)
3. Лимонный сок (нагрев)
4. Раствор щелочи (фенолфталеин).
Нанесли ватной палочкой на листы бумаги надписи различными симпатическими чернилами. При обработке высохших чернил проявителями произошли следующие изменения:
1. Надпись, сделанная крахмалом, при взаимодействии с йодом посинела. Четкого изображения букв было добиться сложно, так как изменял окраску весь лист, на который попадал йод. А именно этот способ тайной передачи информации использовал преступник в рассказе!
2. Надписи молоком и лимонным соком от нагревания потемнели до светло-коричневого цвета.
3. Надпись щелочью, прореагировав с фенолфталеином, приобрела ярко-малиновую окраску. (фотографии 2)
Вывод: наиболее эффективными симпатическими чернилами из рассмотренных в опыте являются раствор щелочи и лимонный сок. В качестве приемлемых чернил для тайнописи можно использовать очень многие из используемых в быту веществ: лекарства, бытовую химию и даже отдельные продукты.
История 3. В «Побеге из тюрьмы Блэкуотер» рассказывается, как заключенный сбежал из камеры, выломав стальной прут оконной решетки. Сломанный прут был значительно тоньше в основании, чем тот, что остался в проеме. Камера освещалась тусклой лампой, работающей от постоянного тока, со скрученными проводами. Лампа располагалась в нескольких футах от окна.
Шерлок Холмс пришел к умозаключению, что сбежавший осуществил электролиз на стальных электродах, используя пищевой уксус, который ему давали для приправы, в качестве электролита. А затем он просто сломал истончившийся прут [4].
Опыт 3. Электролиз раствора уксусной кислоты на растворимых электродах.
Чтобы проверить версию Шерлока Холмса, мы провели собственный эксперимент. Материалы и реактивы: Zn – электроды, разбавленная уксусная кислота, источник тока, амперметр, реостат, провода, прибор для электролиза.
Ход работы: В качестве электролита мы взяли разбавленную уксусную кислоту. Перед началом эксперимента мы взвесили анод и катод. Их масса соответственно равна 27,31 г и 27,16 г. В процессе электролиза на аноде окислялся Zn, на катоде восстанавливались ионы Н+ из уксусной кислоты. Уксусная кислота – слабая, только часть ее молекул в растворе распадается на СН3СОО- и Н+. Ионы Н+ превращаются на катоде в газ Н2. Водород выделяется, растворенный цинк в виде ионов соединяется с ацетат-анионами, образуя соль, часть его, как мы заметили, осаждается на катоде. После повторного взвешивания выяснилось, что масса анода уменьшилась (18,91г), а катода увеличилась (стала 28,9 г) (фото 3).
Уравнения реакций:
Анод (А+): Zn0 –2e > Zn+2
Катод (К-): 2Н+ +2е → Н20^
Суммарное уравнение:
Zn0 + 2H+ → Zn2+ + H20↑
Расчеты по данным нашего эксперимента:
Дано: I ≈ 1,18 A; t= 2 ч = 7200 с; F = 96485 Кл/моль.
Второй закон электролиза Фарадея: для данного количества электричества (электрического заряда) масса химического элемента, осаждённого на электроде, прямо пропорциональна эквивалентной массе элемента. [10] Законы Фарадея можно записать в виде следующей формулы
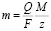 ,
,
где m – масса осаждённого на электроде вещества в граммах; Q – полный электрический заряд, прошедший через вещество; F = 96 485,33(83) Кл•моль -1 – постоянная Фарадея; M – молярная масса вещества; z – число валентных электронов (число электронов на один ион).
Заметим, что M/z – это эквивалентная масса осаждённого вещества.
 г цинка растворится за 2 часа.
г цинка растворится за 2 часа.
Мы процесс проводили 3 дня в течение 2 часов, следовательно, масса растворившегося цинка будет 3• 2,87=8,6 г. Разница при взвешивании равна 27,31-18,91=8,41 г. С учетом потерь, массы примерно одинаковы.
Результат опыта: экспериментально и при помощи расчетов мы подтвердили верность рассуждений Шерлока Холмса о возможности растворения вещества анода при электролизе на растворимых электродах.
Опыт 4. Качественные реакции на соединения железа (II) и (III).
В рассказе Шерлок Холмс доказывал наличие соли двухвалентного железа в составе жидкости, добытой с подоконника камеры, следующим образом. К жидкости он добавлял роданид калия, а затем перекись водорода. Образовывалось вещество кровавого цвета – Fe(SCN)3 – роданид железа (III).
Эта реакция известна как качественная реакция на соединения трехвалентного железа. Нам известно также, что соединения двухвалентного железа окисляются, например, перекисью водорода, и переходят в соединения Fe3+. Еще одна качественная реакция на Fe3+ – это реакция с желтой кровяной солью K4[Fe(CN)6]. [13] В результате образуется темно-синий осадок берлинской лазури (прусская синь) Fe4[Fe(CN)6]3. Эти реакции мы и провели (фото 4).
Материалы и реактивы: штатив с пробирками, FeSO4, FeCl3, KSCN, K4[Fe(CN)6], H2O2.
1) 2FeSO4 + H2O2 + H2SO4 → Fe2(SO4)3 + 2H2O
2) Fe2(SO4)3 + 6 KSCN → 2Fe(SCN)3 + 3K2SO4
3) 4FeCl3 + 3K4[Fe(CN)6] → Fe4[Fe(CN)6]3 ↓ +12KCl
Реакция, описанная в рассказе:
2Fe(CH3COO)2 + 6KSCN + H2O2 + 2CH3COOH → 2Fe(SCN)3 + 6 CH3COOK +2H2O кроваво-красный
Результат опыта: используя качественные реактивы, можно распознать растворы двух- и трехвалентного железа. Доказали, что описанные в рассказе качественные реакции действительно протекают.
Заключение
Шерлок Холмс является одним из самых популярных литературных героев. К решению любой задачи он относится как философ, как художник, как поэт. Чем труднее проблема, тем более она ему интересна. В большинстве случаев Холмс сталкивается с тщательно спланированными и сложно исполненными преступлениями. Но знания химии и других наук позволяют ему найти разгадки даже самых запутанных дел.
Я убедилась, что все описанные в рассказах свойства и превращения веществ, верны с научной точки зрения и не являются художественным вымыслом авторов.
Библиографическая ссылка
Ахмина П.В. ПО СЛЕДАМ ШЕРЛОКА ХОЛМСА И ДОКТОРА ВАТСОНА... // Международный школьный научный вестник. 2019. № 1-4. ;URL: https://school-herald.ru/ru/article/view?id=920 (дата обращения: 19.07.2025).
