Введение
Вся материя состоит из атомов. Авторство возникновения этой теории чаще всего приписывается Демокриту (460-370 до н.э.). Хотя их идеи об атомах были рудиментарными по сравнению с нынешней концепцией сегодня, они обрисовал важную идею, состоящую в том, что все состоит из атомов – невидимых и неделимых сфер материи бесконечного типа и числа.
С греческого «атом» переводится как «неделимый». Долгое время термины «атом», «корпускула», «молекула» были почти синонимами. Ясность внесли химики всего мира в 1860 году. Ученые приняли решение называть атомами мельчайшие неделимые частицы вещества. Если химически устойчивая единица вещества включала в себя несколько атомов, то соответственно говорилось о том, что вещество состоит из молекул.
Нам стало интересно, какую форму имеют разные молекулы, как атомы располагаются в пространстве в различных молекулах, как выглядит молекулы окружающих нас веществ. Поэтому мы решили создать несколько простых, но разнообразных по пространственному строению учебных моделей молекул.
Целями нашей работы можно назвать изучение строения различных молекул и создание масштабных моделей, отражающих их реальные размеры. На основе моделей создание учебного фильма в формате презентации, освещающий тему молекулярного строения веществ.
Для достижения этих целей, мы поставили следующие задачи:
· найти информацию о молекулярном строении вещества и о линейных размерах молекул некоторых неорганических и органических веществ, подготовить обзор литературы;
· перевести указанные размеры в единый масштаб и сделать чертежи различных молекул в указанном масштабе;
· создать шаростержневые и полусферические модели молекул из фольги, деревянных шпажек и модельного пластилина (застывающего) в указанном масштабе;
· подготовить учебный фильм в формате презентации, в которой объясняется молекулярное строение веществ и показываются молекулы различных веществ, показать фильм учащимся 7-8 классов нашей школы;
· сделать выводы по результатам проекта.
В качестве объектов исследования можно молекулы некоторых органических и неорганических веществ.
Предмет исследования – создание масштабных, объёмных моделей выбранных веществ.
Краткие теоретические сведения о строении молекул.
Молекулярные вещества – это вещества, мельчайшими структурными частицами которых являются молекулы. Все молекулы состоят из атомов, как химически неделимых мельчайших частиц вещества. Атомы имеют свой радиус, упрощенно их можно представить в виде сферы. Атомы в молекулах связаны друг с другом химическими связями, тем самым достигается прочность молекулы в пространстве и времени. [1] При этом атомы находятся на некотором расстоянии друг от друга, так как ядра атомов имеют одноименные заряды и поэтому отталкиваются. При образовании химической связи в молекуле всегда происходит сближение атомов [5] – расстояние между ними меньше, чем сумма радиусов изолированных атомов. Межъядерное расстояние между химически связанными атомами называется длиной химической связи.
Следовательно, для изображения молекулы [1, 2] необходимо учитывать следующие параметры.
Длина связи. Для обозначения этих расстояний между атомами в молекуле используется понятие ковалентный радиус. В последнее время атомные радиусы и расстояние между атомами принято выражать в пикометрах (пм, 1 пм = 10-12м). Ранее длину связей представляли в ангстремах (Å, 1Å = 100пм).
Валентные углы. Направление ковалентных связей характеризуется валентными углами – углами между линиями, соединяющими связываемые атомы. Например, в сульфат-ионе SO42- валентные углы между связями сера-кислород равны 109,5°.
Совокупность длин связей и валентных углов в химической частице определяет её пространственное строение. Для определения валентных углов используют экспериментальные методы изучения структуры химических соединений. Оценить значения валентных углов можно теоретически, исходя из электронного строения химической частицы. [4]
Существуют следующие основные геометрические формы молекул [6]:
· Линейная; Треугольная; Тетраэдрическая; Тригонально-бипирамидальная; Октаэдрическая.
Данные формы молекул представлены на рисунке 1.
Некоторые молекулы не укладываются в данную классификацию и имеют свою уникальную форму.
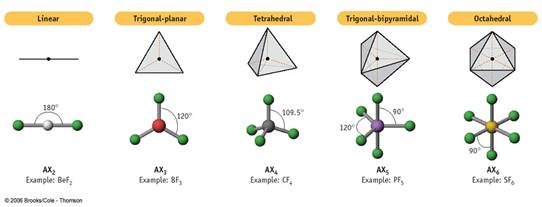
Рисунок 1. Основные формы молекул (слева направо: линейная, треугольная, тетраэдрическая, тригонально-бипирамидальная, октаэдрическая.)
Краткие теоретические сведения о способах представления (моделирования) молекул.
Можно сказать, что молекула – это группировка взаимосвязанных атомов различных химических элементов, поэтому атомы при сближении должны каким-то образом друг с другом связаться, чтобы молекула была устойчива в пространстве [1, 5]. Для молекул характерна только ковалентная связь.
Этот способ образования химической связи заключается в обобществлении внешних электронов. При сближении нескольких атомов отдельные электроны, находящиеся на внешней электронной оболочке, престают принадлежать какому-то одному атому, а становятся общими для двух атомов. Такие электроны называются валентными [1, 4].
Молекулы всегда имеют постоянный состав, подчиняясь закону постоянства состава – закону Пруста (Ж. Л. Пруст, 1801—1808 гг.). [7]
Объединяясь в молекулу, атомы образуют определённую 2D или 3D-структуру (треугольник, квадрат, тетраэдр, октаэдр и т.д.). Данная структура устойчивая и единственно возможная для каждого отдельного соединения. Проще говоря – каждая молекула одного вещества (например: воды) имеет одни и те же размеры и выглядит одинаково. [7, 8]
Для наглядного изображения пространственного строения молекул применяют различные модели: шаростержневая модель, полусферическая модель Стюарта-Бриглеба, модель Драйдинга. [3, 2]
Практическая часть: создание чертежей.
Мы для своего проекта выбрали вещества молекулярного строения, потому что единицей такого вещества является молекула, имеющая постоянные линейные размеры и форму. Для реализации нашего проекта мы выбрали 12 веществ, среди которых взяли некоторые неорганические и органические вещества, которые упоминаются в школьном курсе химии и будут знакомы и интересны учащимся. Вот эти вещества:
водород Н2; кислород О2; озон О3; азот N2; вода H2O; аммиак NH3; угарный газ СО; углекислый газ СО2; метан СН4; этилен С2Н4; бензол С6Н6; ромбическая сера S8.
Также мы постарались выбрать вещества разнообразные и интересные по строению молекулы, чтобы можно было рассмотреть различную форму молекул.
Мы собрали информацию о размерах молекул и валентных углах между отдельными атомами. Далее мы перевели все линейные размеры молекул в масштабе в 5см 0,1нм, кроме молекулы ромбической серы – масштаб в 2,8см 0,1нм. Сводные данные представлены в таблице 1.
Таблица 1. Линейные размеры молекул и вычисление размеров молекул, исходя из выбранного масштаба.
|
Формула вещества |
Длина связей (нм) |
Радиус атома (нм) |
Валент-ный угол, градусы |
Длина связей в масштабе (сантиметры) |
Радиус атома в масштабе (сантиметры) |
|
H2 |
0,074 |
0,053 |
180 |
(0,074*5)/0,1=3,7 |
(0,053*5)/0,1= 2,65 |
|
O2 |
0,121 |
0,06 |
180 |
(0,121*5)/0,1=6,05 |
(0,06*5)/0,1=3 |
|
O3 |
0,128 |
0,06 |
116,8 |
(0,128*5)/0,1=6,4 |
(0,06*5)/0,1=3 |
|
N2 |
0,11 |
0,065 |
180 |
(0,11*5)/0,1=5,5 |
(0,065*5)/0,1=3,25 |
|
H2O |
0,096 |
H-0,053 O-0,06 |
104,45 |
(0,096*5)/0,1=4,8 |
(0,053*5)/0,1=2,65 (0,06*5)/0,1=3 |
|
NH3 |
0,1017 |
N-0,065 H-0,053 |
107 |
(0,1017*5)/0,1=5,9 |
(0,065*5)/0,1=3,25 (0,053*5)/0,1=2,65 |
|
CO |
0,113 |
C-0,07 O- 0,06 |
180 |
(0,113*5)/0,1=5,65 |
(0,07*5)/0,1=3,5 (0,06*5)/0,1=3 |
|
CO2 |
0,116 |
C-0,07 O-0,06 |
180 |
(0,116*5)/0,1=5,8 |
(0,07*5)/0,1=3,5 (0,06*5)/0,1=3 |
|
CH4 |
0,1087 |
C-0,07 H-0,053 |
109 |
(0,1087*5)/0,1=5,4 |
(0,07*5)/0,1=3,5 (0,053*5)/0,1=2,65 |
Продолжение таблицы 1. Линейные размеры молекул и вычисление размеров молекул, исходя из выбранного масштаба.
|
Формула вещества |
Длина связей (нм) |
Радиус атома (нм) |
Валент-ный угол, градусы |
Длина связей в масштабе (сантиметры) |
Радиус атома в масштабе (сантиметры) |
|
C2H4 |
М/д С-0,133 М/д С и Н-0,108 |
C-0,07 H-0,053 |
120 |
(0,133*5)/0,1=5,65 (0,108*5)/0,1=5,4 |
(0,07*5)/0,1=3,5 (0,053*5)/0,1=2,65 |
|
C6H6 |
0,140 |
C-0,07 H-0,053 |
120 |
(0,140*5)/0,1=7 |
(0,07*5)/0,1=3,5 (0,053*5)/0,1=2,65 |
|
S8 |
0,206 |
0,1 |
108 |
(0,206*2,8)/0,1=4,4 |
(0,1*2,8)/0,1=2,8 |
После этого, используя полученные данные, мы начертили модели на бумаге. Для контрастности мы раскрасили атомы в соответствующие цвета, принятые для обозначения различных элементов в химии.
Практическая часть: создание моделей молекул.
Используя чертежи, мы перешли непосредственно к созданию объемных моделей молекул. Для изготовления моделей мы применяли:
· Алюминиевую фольгу для наполнения (придания объема) атомам;
· Легкий пластилин (застывающий) для формирования оболочки атомов;
· Деревянные шпажки для конструирования связей в молекуле.
· Для измерения длины мы использовали линейку, для измерения углов – транспортир.
Первоначально мы сминали фольгу и измеряли заготовки по чертежу (первоначальная подгонка), когда шары из фольги становились сходными по размеру с чертёжными, мы покрывали их пластилином определённого цвета, добиваясь соответствия размеру.
Затем мы брали деревянные шпажки, обрезали их под нужный размер, оставляя место для крепления в атомы, затачивали один из концов ножницами и крепили их в готовые атомы под определённым углом. Углы измеряли транспортиром. Примеры полученных моделей представлены ниже на рисунках 2-5 (шаростержневые модели) и на рисунках 6-7 (полусферические модели). Для того, чтобы ребятам впоследствии можно было подержать в руках наши модели, мы в большинстве молекул заменили тонкие шпажки на деревянные рейки с применением клея.

Рисунок 2. Масштабные модели молекул воды Н2О, озона О3 и водорода Н2 с использованием деревянных реек.

Рисунок 3. Масштабная модель молекулы аммиака NH3

Рисунок 4. Масштабная модель молекулы углекислого газа СО2

Рисунок 5. Масштабная модель молекулы ромбической серы S8
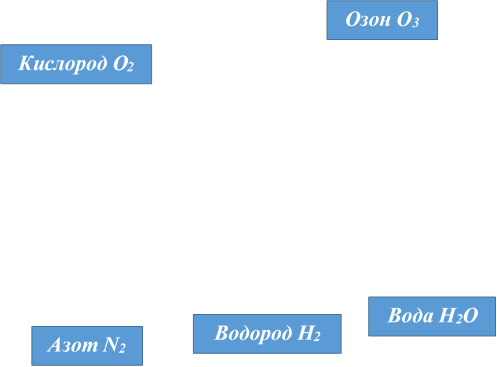

Рисунок 6. Масштабные полусферические модели молекул воды Н2О, озона О3, кислорода О2,азота N2 и водорода Н2.
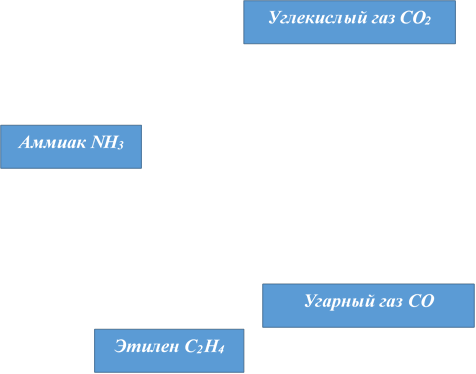

Рисунок 7. Масштабные полусферические модели молекул углекислого газа СО2, угарного газа СО, этилена С2Н4 и аммиака NН3.
Выводы по результатам проекта.
В результате наших исследований мы можем сделать следующие выводы:
· большое количество веществ нашей Вселенной имеет молекулярное строение, то есть состоит из отдельных, устойчивых во времени и пространстве молекул;
· все молекулы имеют разный размер, зависящий от количества атомов в молекуле, характеристик этих атомов, характера химических связей и ее длины;
· состав молекул, а также их форма напрямую влияют на свойства вещества, которое образовано этими молекулами;
· форма некоторых молекул симметрична и уникальна;
· наглядные пособия, которые у нас получились можно использовать при изучении атомно-молекулярного учения, молекулярного строения веществ и т.д.;
· не всегда валентность совпадает с количеством связей в молекуле.
Практическая часть: создание учебного фильма.
При использовании возможностей программы PowerPoint и Word нами был разработан и выполнен учебный фильм. Фильм был показан на уроках по внеурочной деятельности Химическая лаборатория 7а, 7б, 8а и 8к классам. Фильм вызвал большой интерес ребят.
Заключение
Одним из основополагающих понятий современной науки и материалистического представления об устройстве Вселенной является понятия атома и молекулы. На международном съезде химиков в Карлсруэ (Германия) в 1860 году были официально приняты определения этих понятий. Данное введение дало последующий толчок к развитию не только химии и физики, но и других естественных наук. Постепенно, с открытием химического состава молекул (химической формулы) и разработками более совершенных методов исследования строения вещества, были получены знания о размерах и форме тех или иных молекул. Стало возможно построение молекулярных моделей.
Молекулярные модели дают наглядное представление о том, как именно устроены молекулы, а зная эти особенности легко понимать особенности физических и химических свойств вещества. На основании знаний о физических и химических свойствах можно предсказать строение молекул веществ, в ней участвующих. Также противоположное заключение тоже будет верным: на основании сведений о строении молекулы вещества реально предсказать его поведение во время химической реакции.
Разрабатывая свой проект, мы сперва не ожидали большого эффекта, но постепенно увлеклись и создали достаточно большой набор наглядных пособий моделей разнообразных неорганических и органических молекул. Наши пособия позволили нам создать учебный фильм, который дает учащимся возможность окунуться в микромир, увидеть какими причудливыми бывают порой молекулы. А самым любопытным учащимся мы даем возможность потрогать, подержать в руках и поближе рассмотреть наши модели.
Так как учение о молекулах для химической науки является одним из самых главных, то наш проект, надеемся, даст учащимся возможность лучше понять и изучить важнейшие сведения о составе и свойствах этой мельчайшей единицы вещества.
В будущем мы хотели бы продолжить свои исследования и может быть попытаться создать модель природных и искусственных макромолекул (полимеров) в нескольких масштабах, а также дополнить коллекцию примерами других интересных молекул.
Библиографическая ссылка
Шульженко М.А., Денисов М.А. МАСШТАБНОЕ МОДЕЛИРОВАНИЕ МОЛЕКУЛ // Международный школьный научный вестник. 2021. № 3. ;URL: https://school-herald.ru/ru/article/view?id=1455 (дата обращения: 14.05.2026).
