Введение
Реакции с участием радикальных частиц на протяжении многих лет активно используются для синтеза новых веществ и высокотехнологичных материалов на их основе. При этом особая роль свободным радикалам отводится в процессах получения высокомолекулярных соединений и макромолекул с заданным комплексом свойств и характеристик, включая наноразмерные полимерные структуры. Неслучайно именно радикальная полимеризация в настоящее время является основным методом синтеза гомо и сополимеров в промышленности.
Цель работы – изучение ингибиторов и инициаторов радикальных реакций в органической химии и биохимии.
Задачи работы: дать определение радикальным реакциям, инициаторам радикальных реакций, ингибиторам радикальных реакций, определить роль инициаторов и ингибиторов в радикальных реакциях.
Предмет исследования – молекулы органических веществ
Методы исследования: В качестве основного метода исследования используется описание данных о химических реакциях веществ, а также логических выводов, сделанных на основе знаний человечества о химии.
Радикальные реакции
Реакции, в которых происходит гомолитический разрыв связей и образуются свободно-радикальныепромежуточные частицы называются радикальными реакциями.
Гомолитический разрыв связи –это такой разрыв химической связи, когда каждый атом получает при разрыве связи по одному электрону из общей электронной пары.
Образующиеся при этом частицы — это свободные радикалы.
Свободные радикалы –это частицы, каждая из которых содержит один неспаренный электрон.
A:B→A∙ + ∙B
Гомолитический разрыв связихарактерен для слабо полярных или неполярных связей.
Условия протекания радикальных реакций:
· Повышенная температура;
· Неполярный растворитель или отсутствие растворителя
· Реакция протекает под действием света или ультрафиолетового излучения
· В системе присутствуют свободные радикалы или источники свободных радикалов.
Например,взаимодействие метана с хлором протекает по цепному радикальному механизму.
То есть реакция протекает как цепь последовательных превращений с участием свободных радикалов.
Свободные радикалы R∙– это атомы или группы связанных между собой атомов, которые содержат один или несколько неспаренных электронов. Свободные радикалы – очень активные частицы, которые стремятся образовать связь с каким-либо другим атомом [1]..
Этапы радикально-цепного процесса
Стадия 1.Инициирование цепи.Под действием кванта света или при нагревании молекула галогена распадается на радикалы:
Cl:Cl → Cl⋅ + ⋅Cl
Стадия 2.Развитие цепи.Радикалы взаимодействуют с молекулами с образованием новых молекул и радикалов. Радикал галогена взаимодействует с молекулой алкана и отрывает от него водород. При этом образуется промежуточная частица – алкильный радикал, который в свою очередь взаимодействует с молекулой хлора:
CH4+ ⋅Cl → CH3⋅ + HCl
CH3⋅ + Cl2→ CH3Cl + ⋅Cl
Стадия 3. Обрыв цепи.При протекании цепного процесса рано или поздно радикалы сталкиваются с радикалами. При этом образуются молекулы, т.е. радикальный процесс обрывается. Могут столкнуться разные радикалы, в том числе два метильных радикала:
CH3⋅ + ⋅CH3→ CH3CH3
CH3⋅ + ⋅Cl→ CH3Cl
Инициаторы радикальных реакций
Рассмотрим подробнее условия, которые способствуют или, напротив, тормозят образование свободных радикалов.
Вещества, представляющие собой источники свободных радикалов и способствующие развитию радикального процесса, называютинициаторамирадикальных реакций.
Эффективными инициаторами радикальных реакций в органическом синтезе являются производные пероксида водорода: диалкилпероксиды R–O–O–R и гидропероксиды R–O–O–H.
Эти соединения получают алкилированием или ацилированием пероксида водорода.
Эффективность пероксидов в качестве инициаторов радикальных реакций определяется тем, что в их структуре имеется связь О–О, отличающаяся невысокой прочностью. Энергия этой связи в различных пероксидах изменяется от 140 до 200 кДж/моль (30–50 ккал/моль).
Вследствие этого пероксиды весьма неустойчивы даже при комнатной температуре, а при нагревании до 60–80 °С начинают активно разлагаться.
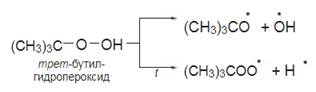
Радикалы, образующиеся при распаде пероксидов, не внедряются в продукты радикальных реакций. Они действуют лишь как источники свободных радикалов и ответственны за инициирование радикального процесса. Например, при действии алкоксидного радикала-инициатора на углеводород R–H образуется радикал R•:
(CH3)3CO•+ R–H (CH3)3COH + R•
(CH3)3COH + R•
Температура, при которой начинает разлагаться пероксид, выступающий в качестве инициатора, определяет то ее значение, при котором следует проводить соответствующую радикальную реакцию.
Распаду пероксидов способствует также УФ-облучение:
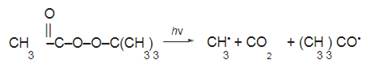
Фотоинициирование радикальных реакций возможно и в отсутствие пероксидов, если среди реагентов имеются молекулы, содержащие в своей структуре слабые связи, например галоген–галоген:
hν
Cl2 2Cl•
2Cl•
Кроме пероксидов в качестве инициаторов радикальных реакций применяют как симметричные, так и несимметричные азосоединения. Эффективность этих инициаторов определяется высокой стабильностью молекулы азота и как следствие — энергетической выгодностью реакций, сопровождаемых его отщеплением. Температура, при которой начинает разлагаться азосоединение, определяется строением радикалов R и R'. Если образуются устойчивые радикалы, азосоединение начинает распадаться уже при 60 °C.
Вместе с тем азометан, например, устойчив при нагревании даже при 400 °С, поскольку метильные радикалы являются крайне неустойчивыми.
Радикальные реакции часто протекают и в живых системах, так как молекулярный кислород является одним из самых распространенных радикалов и сам способен инициировать радикальные реакции. Известно, что в основном состоянии молекула кислорода представляет собой бирадикал, в котором на каждом атоме кислорода находится по одному неспаренному электрону. Как и другие радикалы, кислород может отрывать Н-атом от углеводородного фрагмента и выступать таким образом одним из инициаторов радикальных реакций. В качестве примера можно назвать процессы горения, а также автоокисления, в том числе и в биологических системах [1,3].
Ингибиторы
Эти процессы, регулирующие содержание супероксида в живой клетке, показывают, что в соответствующих ситуациях важным является не только инициирование, но иингибированиерадикальных реакций.
Поскольку углеводороды под действием кислорода воздуха способны образовывать свободные радикалы, актуальным является ингибирование процессов автоокисления топлива и смазочных масел при их длительном хранении. Наиболее эффективныеингибиторынайдены среди аминов, фенолов и аминофенолов. Эти ингибиторы «работают» при их содержании в сохраняемом продукте в количестве всего 0,001–0,1%. Их называют такжеантиоксидантами.
Фрагменты полиненасыщенных кислот, входящие в состав растительных масел и некоторых жиров, особенно склонны к легкому образованию радикалов аллильного типа, быстро трансформирующихся в присутствии кислорода воздуха в гидропероксиды. Эти превращения составляют суть процесса автоокисления и потери качества пищевых продуктов.
Аналогичные реакции развиваются в процессах старения полимеров. Для ингибирования окислительных процессов в полимерных материалах применяют 2,6-ди-трет-бутил-4-метилфенол и фенил-n-аминофенол. Производные фенола добавляют во многие пищевые продукты для увеличения срока их сохранности.
Механизм действия ингибитора радикальной реакции основан на том, что он легко образует устойчивый и, следовательно, малореакционноспособный радикал. Такой радикал оказывается своеобразной ловушкой, обрывающей цепной радикальный процесс [2].
Выводы
Ингибирование и инициирование широко используются в органическом синтезе для проведения и регулирования скорости радикальных реакций.
Радикальные реакции – это реакции, в которых происходит гомолитический разрыв связей и образуются свободно-радикальныепромежуточные частицы.
Инициаторырадикальных реакций – это вещества, представляющие собой источники свободных радикалов и способствующие развитию радикального процесса.
Ингибиторырадикальныхцепныхреакций–этовещества, замедляющие цепныерадикальныереакции.
Современные методы радикальных реакций успешно применяются не только в лабораторной практике для получения новых экспериментальных материалов с улучшенными характеристиками и свойствами, но и внедрены в практику на ряде крупнотоннажных производств.
Библиографическая ссылка
Каменских И.Д. ИНГИБИТОРЫ И ИНИЦИАТОРЫ РАДИКАЛЬНЫХ РЕАКЦИЙ В ОРГАНИЧЕСКОЙ ХИМИИ И БИОХИМИИ // Международный школьный научный вестник. 2023. № 1. ;URL: https://school-herald.ru/ru/article/view?id=1546 (дата обращения: 23.04.2026).
