В воде поверхностных источников помимо неорганических веществ содержатся также и органические соединения, которые можно разделить на природные (гуминовые, фульвокислоты и т.д.) и техногенные (образующиеся в результате человеческой деятельности). Кроме этого возможно наличие патогенных бактерий и вирусов. В настоящее время в полевых условиях для очистки загрязненной воды до состояния «питьевой» используют множество специальных таблеток. Наибольшая популярность принадлежит составам, содержащим хлор или йод. Однако проблема загрязнения окружающей среды стоит очень остро и привычных составов становится недостаточно. Об этом говорит даже тот факт, что в почве, воде, в человеческих органах все чаще обнаруживается «микропластик» (синтетические органические вещества). Поэтому учеными приветствуются все возможные креативные взгляды и идеи решения.
Известно, что в сельской местности для очистки воды издавна используют растения, произрастающие на берегах ручьев, рек, озер. В частности, исследователи Иркутского государственного университета описали возможность очистки сточной воды от металлов и органики корневой системой трав (они используют эти вредные примеси в качестве своего питания [1]). Аналогичные эксперименты проводят и ученые из США по избавлению от «микропластика» [2].
Актуальную тему поддержали студенты УРФУ. Они провели интересный эксперимент: использовали растения для очистки воды, при этом в качестве воды взяли дистиллированную. И на удивление оказалось, что состояние получившейся воды не соответствует требованиям СанПиН [3]. При чем оно отличается от нормы именно в тех параметрах, которые отвечают за наличие органических соединений. Из чего можно сделать вывод, что растения не только убирают, но и отдают большое количество органических соединений в воду.
Такой механизм очистки действительно вызывает интерес. Исследователи объясняют его действенность в основном сорбцией, но мы предполагаем, что нельзя исключить и само по себе взаимодействие органических соединений.
Итак, мы поняли, что растения обладают способностью брать из воды и выделять в нее вещества. Но здесь еще важно отметить тот факт, что травы сами по себе не являются безобидными: они во многом используются в фармакологии и имеют противопоказания к применению. Поэтому работая с ними, важно определять допустимую безопасную дозу для человека.
Цель. Оценить возможность очистки воды при помощи растений.
Задача.На модельной системе «дистиллированная вода и растение» определить максимально возможную массу растения для очистки воды, при этом невредящей здоровью человека, а также оценить возможность удаления растением дополнительно введенных органических соединений, загрязняющих воду.
Выбор растения. Постулируем, что необходимо исследовать каждое применяемое для очистки растение отдельно, т.к. при одинаковой массе и одинаковом способе контакта с водой каждое растение будет выделять разное количество растворенных в воде органических веществ. Выбираем одно растение - крапиву. Крапиву по внешнему виду может определить каждый человек. Ее листья обладают сильными фитонцидными свойствами. Известно, что летом в жару в них можно завернуть свежепотрошенную рыбу или мясо, и оно долго не испортится [4]. Крапива как лекарственное растение также имеет обширные показания к применению, в том числе, она используется как противомикробное и противовоспалительное средство. Нами для исследования приобретены в аптеке фильтр-пакеты «Крапивы листья» фирмы «ФармаЦвет».
Приборы. Штатив, микробюретка, пипетка, мерные колбы объемом на 1 л и на 0,025 л, плоскодонные колбы для титрования, пробирки.
Определение безопасной для человека массы растения необходимой для очистки 1 л воды. В России крапива с ранней весны до глубокой осени служит питательной добавкой к самым разнообразным блюдам. Рекомендуют в крапивный суп класть до 500 г травы, фактически без ограничения. Рассмотрим способ применения и дозы, рекомендованные фармацевтами «ФармаЦвет». Два фильтр-пакета (3,0 г) помещают в стеклянную или эмалированную посуду, заливают 100 мл кипятка, накрывают и настаивают 15 минут, периодически надавливая на пакетики ложкой, затем их отжимают. Объем полученного настоя доводят кипяченой водой до 100 мл. Настой принимают по одной столовой ложке 3-4 раза в день. Случаи передозировки не зарегистрированы. Состав настоя: к 3,0 г крапивы добавляют 100 мл воды. Столовая ложка, т.е. 15 мл настоя соответствует использованию 0,45 г (3 х 15/100) массы крапивы. Дневная доза настоя составляет 60 мл (15 х 4), т.е. в пересчете на растение 1,8 г (0.45 х 4), примерно один фильтр-пакет (1,5 г). Фирма «ФармаЦвет» сообщает, что случаи передозировки такого приема до настоящего времени не зарегистрированы. Следовательно, в день можно использовать только один фильтр-пакет. Объем воды меняем: не 80 мл (кипяток), цвет настоя сильно насыщенный зелено-коричневый, а 1000 мл (комнатной температуры), цвет ещё слабо заметен, зеленовато-коричневый. Учитываем, что из растения при увеличении количества растворителя может выделиться больше органических соединений, как и при использовании нагретой кипящей воды.
Выбор метода анализа. Органические вещества, содержащиеся в воде, в аналитических исследованиях определяются показателями [5]: окисляемость перманганатная (ПМО); химическое потребление кислорода (ХПК); биохимическое потребление кислорода (БПК). Выбираем показатель перманганатная окисляемость. ПМО - это интегральный показатель, который характеризует содержание в воде восстановителей (например, Fe2+) и органических веществ, которые полностью или частично окисляются ионом перманганата в условиях кислой или щелочной среды при нагревании. Показатель ПМО показывает количество кислорода эквивалентное количеству перманганат ионов, потребляемых при обработке пробы перманганатом калия при нагревании в кислой среде в мг кислорода, пошедшего на окисление этих веществ, содержащихся в 1дм3 воды. ПМО воды не должна превышать 10,0 мг/л потребленного кислорода. ПМО основана на окислении органических и неорганических веществ, присутствующих в пробе анализируемой воды заданным количеством перманганата калия в сернокислой среде в процессе нагревания (кипячение) с последующим добавлением оксалат-иона в виде раствора оксалата натрия (способ А) или раствора щавелевой кислоты (способ Б) и титровании его избытка раствором перманганата калия. Для конечной оценки качества питьевой воды и результатов очистки обязательно необходима лицензированная лаборатория, где используются эти методы.
Для предварительного анализа органических соединений модельной системы мы используем более простой и быстрый перманганатный метод, отличающийся от указанного выше меньшей точностью и меньшей скоростью окисления веществ.
Методика анализа. При комнатной температуре к 25 мл анализируемого раствора воды добавляют 10 мл раствора серной кислоты (1:3). Полученный раствор титруют 0,01М водным раствором перманганата калия (титрант). Конец титрования определяют по изменению цвета раствора с розового на бесцветный. Розовый цвет не должен исчезать в течении 15 минут. Определяют сколько мл титранта пошло на титрование.
Экспериментальная часть
Опыт 1. Один фильтр-пакет с крапивой массой 1,5 г вскрывают и его содержимое высыпают в стакан, содержащий 1,0 л дистиллированной воды комнатной температуры, и перемешивают. Через 15 минут раствор фильтруют и анализируют согласно представленной методике. На пробу объемом 25 мл тратится 1,3 мл титранта.
Опыт 2. Один фильтр-пакет с крапивой массой 1,5 г опускают в стакан, содержащий 1,0 л дистиллированной воды комнатной температуры, перемешивают. Через 15 минут пакет удаляют из воды. Раствор анализируют. На пробу 25 мл тратится 1,3 мл титранта.
В полевых условиях можно листья крапивы завернуть в салфетку. Вариант «завернутая салфетка» в случае сухой крапивы лучше, чем россыпь (опыт 1), т.к. листья крапивы ломкие, легкие, их трудно отделить от воды, оседают на дно стакана медленно, необходимо фильтрование.
В опыте 1 и опыте 2 на титрование тратится одно и тоже количество титранта. Следовательно, материал фильтр-пакета не является препятствием и не сорбирует выделяемые из растения органические вещества.
Опыт 3. Приготовление по методике фирмы ФармаЦвет. Фильтр-пакет крапивы (1,5 г) помещают в пустой термостойкий стакан и в него заливают 1 л кипящей дистиллированной воды, пакет всплывает на поверхность воды. Периодически помешивают пакет и слегка отжимают стеклянной палочкой (три раза) в течение 15 минут, далее фильтр-пакет отжимают и убирают из водного раствора. После охлаждения раствора воды до комнатной температуры отбирают пробу. Проба, объемом 25 мл имеет насыщенный коричневато-зеленоватый цвет. На пробу 25 мл пошло 2,3 мл титранта. Этот опыт показывает, что нагревание почти в два раза увеличивает выделение органических соединений из растения. Вероятно, но с дополнительной проверкой, объем приготовленной воды с одним пакетом в полевых условиях без использования нагрева и отстаивания может быть увеличен в 1,8 раза (2,3/1,3) т.е. подвергать очистке одним фильтр-пакетом можно примерно 2 литра воды. Необходимо учитывать температуру очищаемой воды.
В качестве органического загрязнителя воды выбран фенол - широко распространенное антропогенное загрязнение. В природных водах содержание фенолов может достигать десятков и даже сотен миллиграммов в 1 л воды. В реках естественный фон не превышает 20 мкг/л. Анализ воды на фенол важен для природных и сточных вод. Для России содержание фенола в питьевой воде не должно превышать 0,001 мг/л [6]. Фенолы - соединения нестойкие и подвергаются биохимическому и химическому окислению. Фенол окисляется до гидрохинона.
Опыт 4. Приготовлен раствор фенола в дистиллированной воде с концентрацией 1г/л. В мерную колбу объемом 25 мл вносят 0,25 мл раствора фенола и доводят до метки колбы дистиллированной водой. На пробу объемом 25 мл, в которой содержится 0,25 мг фенола, потребовалось 0,40 мл титранта. По аналогии, на 0,50 мл раствора фенола требуется 0,80 мл титранта; на 0,75 мл раствора фенола требуется 1,20 мл титранта; на 1,00 мл раствора фенола требуется 1,60 мл раствора титранта.
Опыт 5. Приготовлен раствор фенола в дистиллированной воде с концентрацией 1мг/л. В мерную колбу объемом 25 мл вносят 0,25 мл раствора фенола и доводят до метки водным раствором травы (опыт 2). На пробу объемом 25 мл, в которой содержится 0,25 мг фенола, потребовалось 0,85 мл титранта.
Опыт 6. Приготовлен раствор фенола в дистиллированной воде с концентрацией 1мг/л. В мерную колбу объемом 25 мл вносят 0,50 мл раствора фенола и доводят до метки водным раствором травы (опыт 2). На пробу объемом 25 мл, в которой содержится 0,50 мг фенола, потребовалось 1,35 мл титранта.
Опыт 7. Приготовлен раствор фенола в дистиллированной воде с концентрацией 1мг/л. В мерную колбу объемом 25 мл вносят 0,75 мл раствора фенола и доводят до метки водным раствором травы (опыт2). На пробу объемом 25 мл, в которой содержится 0,75 мг фенола, потребовалось 1,70 мл титранта.
Опыт 8. Приготовлен раствор фенола в дистиллированной воде с концентрацией 1мг/л. В мерную колбу объемом 25 мл вносят 1,0 мл раствора фенола и доводят до метки водным раствором травы (опыт 2). На пробу объемом 25 мл, в которой содержится 1,00 мг фенола, потребовалось 2.10 мл титранта.
Результаты очистки воды от фенолов растворимыми в воде соединениями крапивы изображены графически на рисунке.
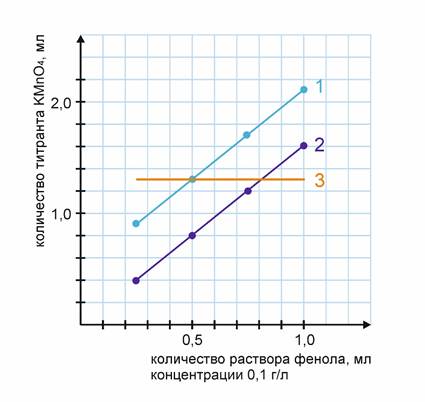
Рисунок. Очистка воды от фенола крапивой.
1 – титрование фенола в настое крапивы объемом 25 мл.
2 – титрование фенола в дистиллированной воде
3 – количество титранта требующееся на объем 25 мл настоя крапивы
Результаты (опыты 5, 6, 7, 8) окисления фенола, помещенного в настой крапивы, полученного в опыте 2, представлены на графике линией 1. Чистый фенол, растворенный в дистиллированной воде (опыт 4), легко окисляется перманганатом калия в кислой среде, линия 2. На объем 25 мл самого настоя должно идти постоянное количество титранта равное 1,3 мл из-за наличия в нем растворенных органических соединений крапивы, данные получены в опыте 2, линия 3. При отсутствии какого-либо взаимодействия фенола и химических соединений настоя травы общее количество титранта достигло бы суммы его затрат на титрование фенола и 25 мл раствора органических соединений, выделенных из крапивы. Однако экспериментально показано, что на совместное титрование настоя крапивы и добавленного в него фенола (линия 1), идет титранта значительно меньше, линия 1 расположена частично даже ниже линии 3. Следовательно, предполагаем, что происходит взаимодействие фенола с органическими соединениями настоя растения. Другими методами убыль фенола нами не определялась.
Экспериментально показано на примере фенола и водного настоя крапивы, что загрязнённая органическими соединениями (фенолом) вода очищается химическими соединениями настоя крапивы, вероятно, фенол и органические соединения взаимодействуют друг с другом, что подтверждается литературными данными об очистке растениями грязных вод до питьевых [7].
Выводы:
1. На модельной системе: дистиллированная вода и листья крапивы определена максимально возможная масса растения равная 1.5г (фильт-пакет листьев крапивы) для очистки воды, объёмом в до 2 л воды в день, не вредящая здоровью человека.
2. Показана возможность удаления крапивой из воды дополнительно введенных органических соединений, загрязняющих воду, на примере фенола. Масса 1,5 г крапивы может «нейтрализовать» 0,50 мг фенола.
3 Предложен косвенный метод оценки определения безопасной для человека массы растения необходимой для очистки воды.
4. Нами подтверждено, что метод использования растений для очистки воды перспективен и требует дальнейшего развития.
Библиографическая ссылка
Ершов М.Д., Животов А.С., Осипова Е.А., Бушланова М.В. ОЧИСТКА ВОДЫ РАСТИТЕЛЬНЫМИ МАТЕРИАЛАМИ // Международный школьный научный вестник. 2025. № 2. ;URL: https://school-herald.ru/ru/article/view?id=1647 (дата обращения: 30.04.2026).
