Введение. Зависимость большинства процессов жизнедеятельности организма от температуры окружающей среды делает температурные воздействия важнейшим фактором экологии, который может иметь решающее значение для выживания человека. С воздействием низких и сверхнизких температур человеку часто приходится встречаться при работе на различных производствах, а также в силу проживания – в некоторых климатических зонах. При этом пребывание организма в условиях гипотермического воздействия может приводить к значительным метаболическим и функциональным изменениям.
В ответ на сверхсильный внешний раздражитель (холод) происходит усиление деятельности важнейших регулирующих систем – нервной и эндокринной. Адаптация организма к влияниям окружающей среды обеспечивается, прежде всего, путем соответствующих изменений, колебаний функциональной активности органов и тканей [1,2].
Критерии смерти от переохлаждения - резкое снижение гликогена в тканях трупа. На данный момент нет достаточно точных данных об изменениях количества гликогена в гепатоцитах после гипотермии и при их регенерации [3,4,5].
Цель исследования: изучить количественные характеристики гликогена в гепатоцитах белых крыс после экспериментальной гипотермии на разных этапах регенерации.
Задачи исследования: рассмотреть динамику изменения интегральной оптической плотности гликогена гепатоцитов в постгипотермальном периоде.
Материалы и методы. Исследование выполнено на 25 крысах линии Wistar. Гипотермию моделировали путем помещения животных, находящихся в индивидуальных клетках, в воду температурой 5 °С, при температуре окружающего воздуха 7 °С. Критерием прекращения воздействия служило достижение животными ректальной температуры 20-25 °С, что соответствовало глубокой степени гипотермии. Время экспозиции было индивидуальным и в среднем составляло 40 ± 5 мин. В ходе эксперимента животные умерщвлялись сразу после прекращения охлаждения, через 2 дня, 5 дней и 14 дней после прекращения охлаждения. Обезболивание и умерщвление животных проводили в соответствии с «Правилами проведения работ с использованием экспериментальных животных».
Материал фиксировали в 10 % нейтральном формалине забуференном по Лилли. Гистологические срезы толщиной 4-7 мкм окрашивали гематоксилином и эозином, на гликоген по Шабадашу. Цифровые микрофотографии препаратов получали с помощью микроскопа Nikon Eclipse E200 (Япония) и цифровой видеокамеры VIDI CAM (Россия). Количество гликогена высчитывали путем определения интегральной оптической плотности (ИОП) полисахарида в условных единицах (у.е.) в морфометрической программе UTHSCSA Image Tool 3.0 (разработанной в University of the Texas Health Science Center of San Antonio, Texas). Статистическую обработку материала проводили при помощи статистического пакета Statistica 6.0.
Собственные результаты
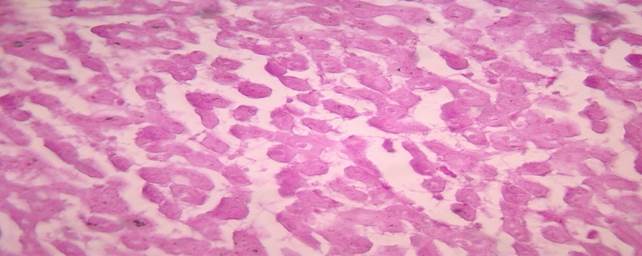
Рис. 1. Сразу после проведения гипотермии гликоген в гепатоцитах определялся в виде «пылевидной» светло-фиолетовой зернистости.
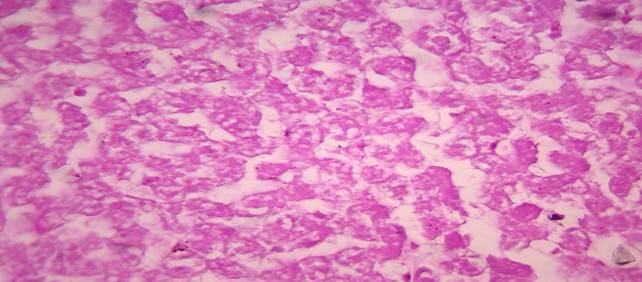
Рис 2. Через 2 дня после гипотермии отмечали неравномерное распределение гликогена по цитоплазме печеночных клеток в виде крупноглыбчатых и мелкоглыбчатых темно-фиолетовых скоплений.
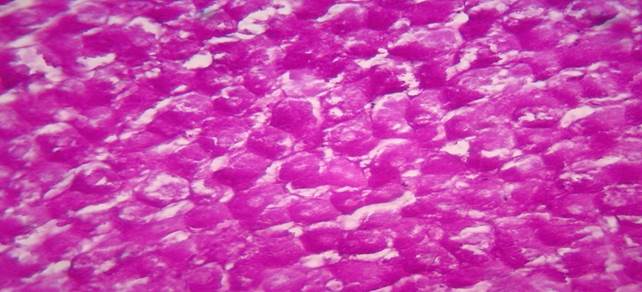
Рис 3. Через 5 дней после гипотермии большинство гепатоцитов печени крыс были переполнены гликогеном, который определялся в виде крупных зерен темно-фиолетово-вишневой окраски.
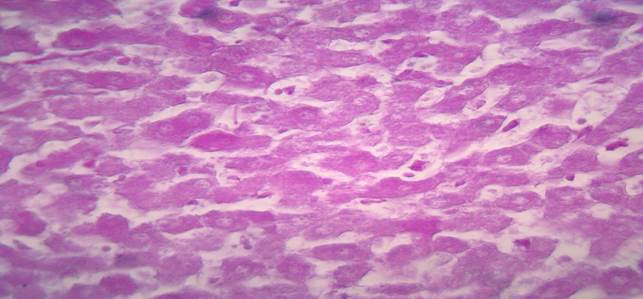
Рис. 4. На 14 день после проведения гипотермии гликоген определяется в виде мелкой слабо-фиолетовой зернистости в цитоплазмах печеночных клеток.
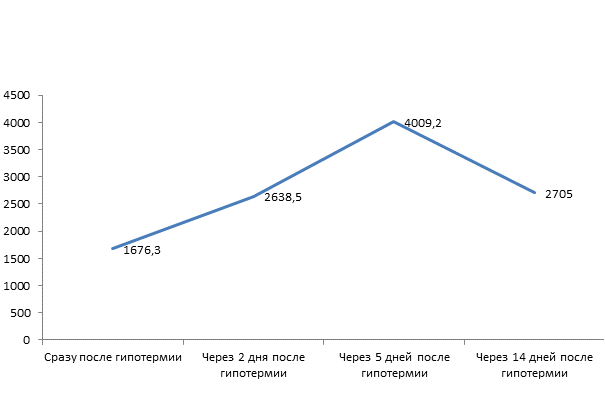
Рис. 5. Динамика изменения плотности гликогена
Заключение. Проведенное исследование позволило сделать несколько выводов:
1. Воздействие гипотермии приводило к уменьшению количества гликогена в клетках печени.
2. В период регенерации клеток печени после гипотермии синтез гликогена возрастал.
3. На 14-ый день эксперимента ИОП гликогена уменьшилась и приходила к норме.
В условиях гипотермии печень как орган, вносящий значительный вклад в термопродукцию, играет очень важную роль. За счет сложных биохимических реакций этот орган способен обеспечивать приспособляемость организма к сложным условиям существования. Печень обеспечивает пластические и энергетические процессы, а также регулирует адаптивные компенсаторно-приспособительные процессы, происходящие при воздействии всех экзогенных и эндогенных неблагоприятных процессов, и эта регуляция осуществляется даже тогда, когда повреждающие факторы не обладают выраженным гепатотропным эффектом. Поэтому морфофункциональное состояние печени является отражением не только функционального состояния самого органа, но и реакции организма в целом.
